Categorieën
nieuwe blog
- Vergelijking van kathodematerialen voor batterijen: NMC, LFP en NCA
- Trends in de productie van lithium-ionbatterijen tot 2026: een B2B-kopersgids
- Stapsgewijze handleiding voor het productieproces van lithium-ionbatterijen
- Belangrijkste oorzaken van lekkage bij het sealen van pouchcellen
- Vorming en sortering in de lithium-ionbatterijproductie
Tags
Amorfe LiSiON dunne-film-elektrolyt voor volledig vaste-stof dunne-film-lithiumbatterij
Auteur: XIA Qiuying, SUN Shuo, ZAN Feng, XU Jing, XIA Hui
Materiaalschool Wetenschap en techniek, Nanjing Universiteit voor Wetenschap en Technologie, Nanjing 210094, China
Samenvatting
All-solid-state dunne-film-lithiumbatterij (TFLB) wordt als het ideaal beschouwd stroombron voor micro-elektronische apparaten. Echter, het relatief lage ionisch De geleidbaarheid van amorfe elektrolyt in vaste toestand beperkt de verbetering van elektrochemische prestaties voor TFLB. In dit werk, amorf lithium-silicium Dunne films van oxynitride (LiSiON) worden vervaardigd door magnetronsputteren vastestofelektrolyt voor TFLB. Met geoptimaliseerde afzettingsomstandigheden kan de De dunne LiSiON-film vertoont een hoge ionische geleidbaarheid van 6,3×10-6 Sâcm-1 in kamerruimte temperatuur en een breed spanningsvenster van meer dan 5 V, waardoor het een geschikte dunne film is elektrolyt voor TFLB. Een MoO3/LiSiON/Li TFLB is dat wel geconstrueerd op basis van de LiSiON dunne film-elektrolyt met grote specifieke capaciteit (282 mAhâg-1 bij 50 mAâg-1), goede snelheid capaciteit (50 mAhâg-1 bij 800 mAâg-1), en acceptabel levensduur (78,1% capaciteitsbehoud na 200 cycli), wat aantoont dat haalbaarheid van dit elektrolyt voor praktische toepassingen.
Zoekwoordenï¼ LiSiON; dunne film elektrolyt; volledig solid-state lithiumbatterij; dunnefilmbatterij
De snelle ontwikkeling van de micro-elektronica-industrie, zoals micro-elektromechanische systemen (MEMS), microsensoren, intelligente kaarten, en implanteerbare micromedische apparaten leidt tot een toenemende vraag naar geïntegreerde micro-energieopslag[1,2]. Onder de beschikbare batterijtechnologieën zijn all-solid-state dunne film lithiumbatterij (TFLB) wordt als ideaal beschouwd stroombron voor micro-elektronische apparaten vanwege hun hoge veiligheid, kleine formaat, power-on-chip-ontwerp, lange levensduur en lage zelfontlading. Als een van De belangrijkste componenten in TFLB, solid-state dunne-film elektrolyt, spelen een cruciale rol rol bij het bepalen van de eigenschappen van TFLB[3]. Daarom, Het ontwikkelen van hoogwaardige dunnefilmelektrolyten in vaste toestand is altijd een uitdaging belangrijk doel voor de ontwikkeling van TFLB. Momenteel het meest gebruikt elektrolyt in TFLB is amorf lithiumfosforoxynitride (LiPON), dat heeft een matige ionische geleidbaarheid (2Ã10-6 Sâcm-1), lage elektronische geleidbaarheid (~10-14 Sâcm-1), breedspanning venster (~5,5 V) en goede contactstabiliteit met lithium[4,5]. Echter, het is De ionische geleidbaarheid is relatief laag, wat de toekomstige ontwikkeling van krachtige TFLB voor het komende tijdperk van het Internet of Things (IoT)[6]. Zo is het ook urgent om nieuwe dunne-film elektrolyten te ontwikkelen met verhoogde ionische geleidbaarheid, evenals een groot spanningsvenster en goede contactstabiliteit met lithium voor TFLB van de volgende generatie.
Van de verschillende anorganische elektrolytmaterialen in vaste toestand is de vaste stof Li2O-SiO2 oplossingssysteem en hun deuterogene fasen werden geïdentificeerd als potentieel dun filmelektrolyten vanwege hun snelle driedimensionale lithiumgeleiding kanalen[7]. Chen et al.[8] gemeld dat Al-gesubstitueerde vaste elektrolyt Li4.4Al0.4Si0.6O4-0.3Li2O een hoge ionische geleidbaarheid heeft van 5,4 Ã10-3 Sâcm-1 bij 200 â. Adnan, et al.[9] vond dat Li4Sn0.02Si0.98O4 verbinding heeft een maximale geleidbaarheidswaarde van 3,07×10-5 Sâcm-1 bij omgevingstemperatuur. Echter, eerdere werken aan Li2O-SiO2-elektrolytsystemen waren vooral gericht op poeder materialen met een hoge kristalliniteit, terwijl er over zeer beperkt werk werd gerapporteerd hun amorfe dunne film-tegenhangers voor TFLB. Omdat TFLB dat doorgaans is geconstrueerd door dunne films van kathode-, elektrolyt- en anodelagen aan te brengen laag, moet de elektrolytfilm bij relatief lage temperatuur worden vervaardigd om de ongunstige interacties tussen de kathode en de elektrolyt te vermijden, wat resulteert in barsten en kortsluiting van de TFLB[1,2]. Dus, ontwikkeling van Li2O-SiO2-elektrolyt met amorfe eigenschap, bereid op lage temperatuur temperatuur is belangrijk voor TFLB. Hoewel uit recent werk[6] blijkt dat een hoge lithium-ionische geleidbaarheid van 2,06×10-5 Sâcm-1 kan worden verkregen door amorfe Li-Si-P-O-N dunne film, de contactstabiliteit met de elektroden en elektrochemisch stabiliteit in TFLB moeten nog worden onderzocht. Daarom is het van cruciaal belang Het is belangrijk om hoogwaardige, op Li2O-SiO2 gebaseerde dunnefilm-elektrolyten te ontwikkelen demonstreer de daadwerkelijke toepassing ervan in TFLB.
In dit werk werd een dunne film van amorf lithium-siliciumoxynitride (LiSiON) gebruikt bereid door radiofrequentie (RF) magnetronsputteren bij kamertemperatuur en onderzocht als elektrolyt in vaste toestand voor TFLB. Het sputtervermogen en de stroom van N2/Ar-werkgas werd geoptimaliseerd om de beste afzettingsomstandigheden te verkrijgen voor de LiSiON dunne film. Bovendien, om de toepasbaarheid van de geoptimaliseerde LiSiON-elektrolyt voor TFLB werd een volledige MoO3/LiSiON/Li-cel gebouwd en de bijbehorende De elektrochemische prestaties werden systematisch onderzocht.
1 Experimenteel
1.1 Bereiding van dunne LiSiON-films
Dunne LiSiON-films werden vervaardigd door RF-magnetronsputteren (Kurt J. Lesker) met behulp van een Li2SiO3-doel (diameter 76,2 mm) bij kamertemperatuur 12 uur. Vóór de afzetting werd de druk van de kamer verlaagd tot minder dan 1×10-5 Pa. De afstand van doel tot substraat was 10 cm. De monsters afgezet onder een RF-vermogen van 80, 100 en 120 W bij een stroom van 90 sccm N2 gemarkeerd als respectievelijk monster LiSiON-80N9, LiSiON-100N9 en LiSiON-120N9. En de monsters afgezet onder een RF-vermogen van 100 W bij een stroom van 90 sccm N2 en 10 sccm Ar, 90 sccm N2 en 50 sccm Ar, 50 sccm N2 en 50 sccm Ar zijn gemarkeerd als monster LiSiON-100N9A1, LiSiON-100N9A5 en LiSiON-100N5A5, respectievelijk.
MoO3-film werd bereid met een reactieve magnetron met gelijkstroom (DC). sputteren (Kurt J. Lesker) met behulp van een puur metalen Mo-doelwit (diameter 76,2 mm) volgens ons vorige rapport[10]. De afstand van doel tot substraat was 10 cm, en DC het sputtervermogen bedroeg 60 W. De afzetting werd op het substraat uitgevoerd temperatuur van 100 â gedurende 4 uur bij een stroom van 40 sccm Ar en 10 sccm O2, gevolgd door een in-situ gloeibehandeling bij 450 ºC gedurende 1 uur. LiSiON-100N9A1 werd vervolgens op de MoO3-film afgezet als elektrolyt. Daarna ontstond een metallische lithiumfilm met een dikte van ongeveer 2 µm afgezet op de LiSiON-film door thermische vacuümverdamping (Kurt J. Lesker). De laatste fabricagestap omvatte de afzetting van Cu-stroomcollector en het inkapselingsproces.
De kristalstructuren van de monsters werden gekarakteriseerd door röntgendiffractie (XRD, Bruker D8 Advance). De morfologieën en microstructuren van de monsters werden gekarakteriseerd door veld emissie scanning elektronenmicroscoop (FESEM, FEI Quanta 250F) uitgerust met energiedispersieve röntgenspectroscopie (EDS). De elementaire composities van de monsters werden geanalyseerd met inductief gekoppelde plasmamassaspectrometrie (ICP-MS, Agilent 7700X). De chemische samenstelling en bindingsinformatie van de monsters werden gemeten met röntgenfoto-elektronenspectroscopie (XPS, Escalab 250XI, Thermo Wetenschappelijk).
1.4 Elektrochemische metingen
De ionische geleidbaarheid van de LiSiON dunne-film-elektrolyt werd gemeten met behulp van een ingeklemde structuur van Pt/LiSiON/Pt. De elektrochemische impedantie spectroscopie (EIS) (van 1000 kHz tot 0,1 Hz met potentiële amplitude van 5 mV) en cyclische voltammetrie (CV) metingen van de monsters werden uitgevoerd op de Biologisch VMP3 elektrochemisch werkstation. Galvanostatische lading/ontlading (GCD) meting van de MoO3/LiSiON/Li TFLB werd uitgevoerd met behulp van een Neware BTS4000 batterijsysteem in een met argon gevuld handschoenenkastje bij kamertemperatuur. Een Sartorius Analytische balans (CPA225D, met resolutie van 10 µg) werd gebruikt om te bepalen de massabelasting van de elektrode en de massabelasting van de MoO3-film zijn ongeveer 0,4 mgâcm-2.
2 Resultaten en discussie
Zoals weergegeven in de optische afbeelding ingevoegd in figuur 1(a), a Li2SiO3-doelwit werd gebruikt om LiSiON-dunne film te bereiden. Het XRD-resultaat in figuur 1(a) onthult dat het doelwit bestaat uit de belangrijkste Li2SiO3 (JCPDS 83-1517) fase en kleine SiO2-fase. ICP-MS-meting geeft aan dat de atomaire verhouding van Li: Si is ongeveer 1,79: 1 in het doel. Transparant amorf dun film werd verkregen voor het typische monster LiSiON-100N9A1 na sputteren doel (Fig. 1 (b)). De dikte van het typische monster LiSiON-100N9A1 gemeten vanaf de dwarsdoorsnede FESEM-afbeelding in figuur 1 (c) is ongeveer 1,2 µm, wat wijst op een groeisnelheid van ongeveer 100 nmâh-1 onder deze toestand. Zoals weergegeven in de FESEM-afbeelding in bovenaanzicht in figuur 1(d), is de oppervlak van de LiSiON dunne film is zeer glad en dicht, zonder scheuren of gaatjes, waardoor het een geschikte vaste elektrolyt is voor TFLB om kortsluiting te voorkomen veiligheidsprobleem.
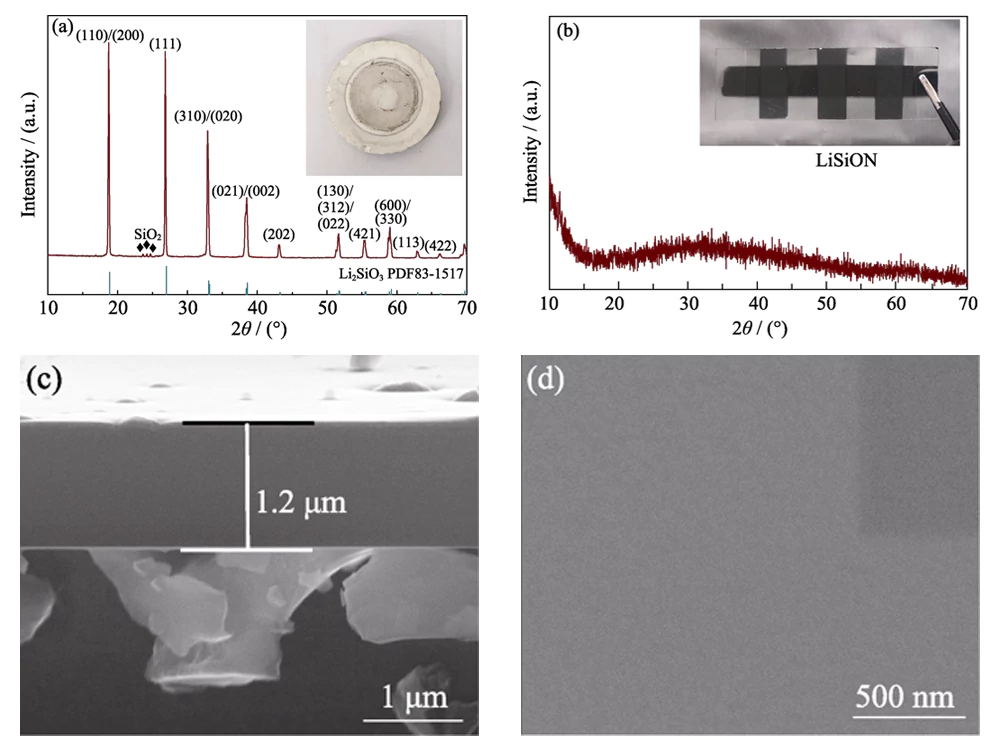
Fig. 1 (a) XRD-patroon en optisch beeld van het Li2SiO3-doel; (b) XRD-patroon en optisch beeld van typisch monster LiSiON-100N9A1; (c) Dwarsdoorsnede en (d) FESEM-afbeeldingen van bovenaf van het typische monster LiSiON-100N9A1
Er werd XPS-analyse uitgevoerd om de chemische samenstelling te onderzoeken bindingsinformatie van het Li2SiO3-doel en het typische monster LiSiON-100N9A1. Het XPS-onderzoek scanspectra in figuur 2 (a) onthullen de aanwezigheid van Li-, Si- en O-elementen in het Li2SiO3-doelwit en de introductie van het N-element in de dunne LiSiON-film. De atoomverhouding van N: Si in LiSiON dunne film is ongeveer 0,33: 1 volgens het XPS-resultaat. Gecombineerd met de overeenkomstige atoomverhouding (1,51: 1) verkregen door de ICP-MS meting is de stoichiometrie van het typische monster LiSiON-100N9A1 bepaald als Li1.51SiO2.26N0.33. Vergeleken met de enkele Si-Si (103,2 eV) piek in de Si2p XPS-spectrum op kernniveau van het Li2SiO3-doel (Fig. 2 (b)), extra Si-N (101,6 eV) piek kan worden waargenomen uit de dunne LiSiON-film, wat suggereert dat er sprake is van nitridatie in LiSiON[11,12]. De O1's XPS-spectrum op kernniveau van Li2SiO3-doelwit in figuur 2 (c) toont twee bindingsomgevingen: 531,5 eV is afkomstig van SiOx en 528,8 eV toegewezen aan Li2O. Na afzetting kwam er een extra component naar voren bij 530,2 eV kan worden waargenomen met dunne LiSiON-film, die kan worden toegeschreven aan niet-overbruggend zuurstof (Aan) in silicaat[13,14]. Het N1s XPS-spectrum op kernniveau van LiSiON dunne film in figuur 2(d) kan worden gedeconvolueerd in drie pieken, waaronder 398,2 eV voor Si-N-binding, 396,4 eV voor Li3N, en 403,8 eV voor nitrietsoorten NO2-, wat de opname van N in de LiSiON-netwerk[14,15,16]. Zoals schematisch geïllustreerd in figuur 2(e), is de opname van N in het LiSiON-netwerk kan meer verknoopt zijn structuur, wat gunstig is voor snelle geleiding van lithiumionen[6,17].
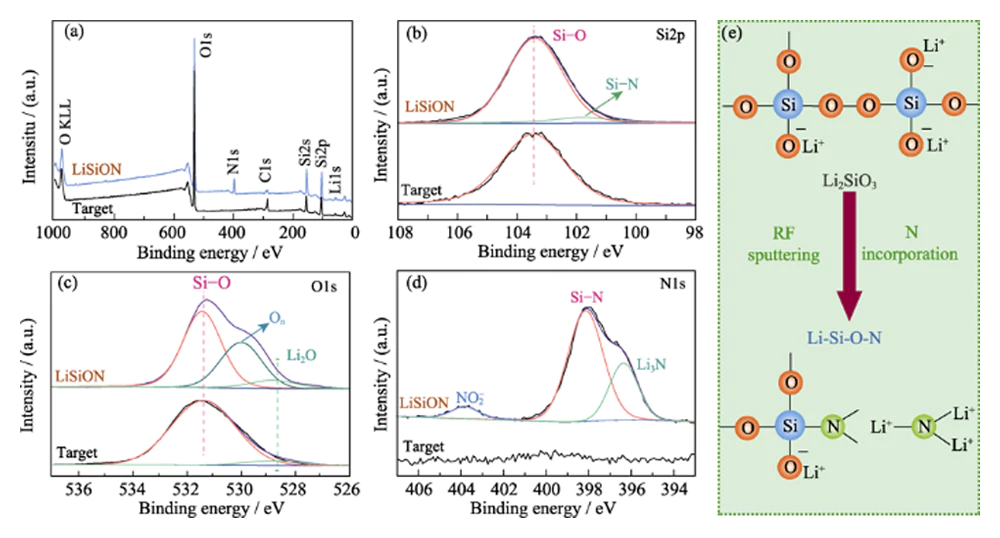
Afb. 2 (a) Enquêtescan, (b) Si2p-kernniveau, (c) O1s-kernniveau, en (d) N1s XPS-spectra op kernniveau van Li2SiO3-doelwit en typisch monster LiSiON-100N9A1; (e) Schematische weergave van de gedeeltelijke structuurverandering van Li2SiO3 naar LiSiON met de integratie van N
Om de ionische geleidbaarheid en elektrochemische stabiliteit van de Dunne LiSiON-films, verschillende dunne LiSiON-films afgezet bij verschillende sputteren krachten, en werkgasstromen werden vergeleken in termen van hun ionisch geleidbaarheid en spanningsvensters. De Nyquist-grafieken op kamertemperatuur van de Dunne LiSiON-films worden weergegeven in figuur 3 (a), en de overeenkomstige Pt/LiSiON/Pt-sandwichstructuur en het equivalente circuit zijn dat wel getoond in figuur 3 (b). Als waargenomen vertonen de Nyquist-grafieken een enkele halve cirkel en een diëlektricum capaciteitstaart, die kenmerkend is voor dunnefilmgeleidend diëlektricum met bulk-relaxatieproces ingeklemd tussen blokkerende contacten [17]. Het ionisch geleidbaarheid (Ïi) van de dunne LiSiON-films kunnen worden berekend met behulp van Vgl. (1).
Ïi=d/(RA)
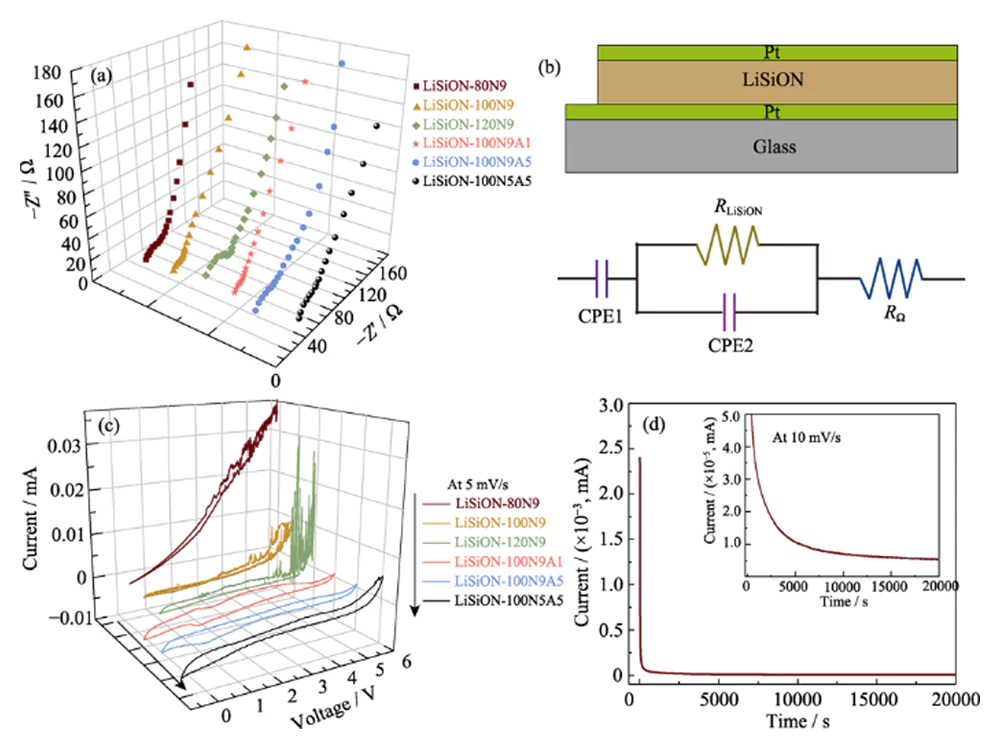
Afb. 3 (a) Elektrochemische impedantiespectroscopie (EIS) spectra van de dunne LiSiON-films afgezet onder verschillende omstandigheden; (b) Schematisch illustratie van de Pt/LiSiON/Pt-sandwichstructuur en de bijbehorende gelijkwaardig circuit; (c) CV-curven van de dunne LiSiON-films die zijn afgezet onder verschillende omstandigheden; (d) Chronoamperometriecurve van het monster LiSiON-100N9A1
waarbij d de filmdikte is, A is de effectief gebied (ongeveer 1 cm2), en R is de geschatte filmweerstand uit de gemeten Nyquist-plot. De berekende ionische geleidbaarheid hiervoor Dunne LiSiON-films worden vergeleken in Tabel 1. Zoals waargenomen is de ionische geleidbaarheid van de afgezette LiSiON-dunne film bij een constante stroom van 90 sccm neemt N2 toe met het toenemende sputtervermogen vanaf 80 W tot 100 W, en neemt vervolgens af wanneer het sputtervermogen verder wordt verhoogd tot 120 W, vergelijkbaar met het vorige rapport over LiPON-elektrolyt[18]. Een voor de hand liggende Een toename van de ionische geleidbaarheid kan worden waargenomen wanneer de N2-verhouding in het werkgas wordt onder een constant sputtervermogen van 100 W bevorderd, waardoor kan worden toegeschreven aan de toegenomen hoeveelheid opgenomen stikstof in de LiSiON met een gunstiger omgeving voor de beweging van lithiumionen[5, 18]. Merkbaar, het monster LiSiON-100N9 en LiSiON-100N9A1 vertonen de hoogste ionische geleidbaarheid van respectievelijk 7,1×10-6 en 6,3×10-6 Sâcm-1, die duidelijk hoger zijn dan het bekende LiPON (~2×10-6 Sâcm-1), eerder gerapporteerde amorfe LiNbO3 (~1×10-6 Sâcm-1)[19], LiBON (2,3×10- 6 Sâcm-1)[20], Li-V-Si-O (~1x10-6 Sâcm-1)[21], Li-La-Zr-O (4x10-7 Sâcm-1)[22] en Li-Si-P-O (1,6×10-6 Sâcm-1)[23] elektrolytfilms, waaruit blijkt dat de amorfe LiSiON dunne film is een concurrerende kandidaat als elektrolyt voor TFLB. De hoge ionengeleidbaarheid van de dunne LiSiON-film kan worden toegeschreven aan de integratie van N in de dunne film en de vorming van Si-N-bindingen in plaats van Si-O-bindingen, wat leidt tot een meer netvormig anionisch netwerk voor het gemakkelijke lithiumion mobiliteit[17, 24]. De elektrochemisch stabiele spanningsvensters van de LiSiON dunne films werden geëvalueerd door CV-meting bij een scansnelheid van 5 mVâs-1 met spanning tot 5,5 V. Er moet op worden gewezen dat de impact van afzetting De toestand van het spanningsvenster van LiSiON-films varieert, wat niet mogelijk is momenteel verklaard door een duidelijk mechanisme, aangezien er geen relevant onderzoek is in eerdere rapporten over dunne-film-elektrolyt[18,24-25]. Hoe dan ook, vergeleken in figuur 3(c) en Tabel 1 toont het voorbeeld LiSiON-100N9A1 en LiSiON-100N5A5 de breedste spanning vensters van respectievelijk ~5,0 en ~5,2 V, die dicht bij die van LiPON liggen elektrolyt. Daarom zijn zowel de ionische geleidbaarheid als het spanningsvenster genomen in overweging werd monster LiSiON-100N9A1 gekozen voor verder onderzoek en de vervaardiging van volledige cellen. Om de overdracht van lithiumionen te onderzoeken getal (Ïi) en de elektronische geleidbaarheid (Ïe) van het monster LiSiON-100N9A1, chronoamperometrie werd verder uitgevoerd bij een constante spanning van 10 mV (figuur 3(d)). De Ïi kan worden berekend met Vgl. (2).
Ïi=(Ib-Ie)/Ib
waarbij Ib de initiële polarisatiestroom is, en Ie de constante huidige status[18]. De Ïi werd berekend op 0,998 dicht bij 1, wat aangeeft dat de geleiding van lithiumionen absoluut dominant is in de elektrolyt. De Ïi wordt bepaald door een gemengd effect van de geleiding van ionen en elektronen [24], wat kan worden uitgedrukt door Vgl. (3).
Ïi=Ïi/(Ïi+Ïe)
De Ïe van het monster LiSiON-100N9A1 wordt dus berekend als 1,26Ã10-8 Sâcm-1, wat verwaarloosbaar is vergeleken met de ionengeleiding.
Tabel 1 Vergelijking van de geleidbaarheid en spanning van lithiumionen vensters van dunne LiSiON-films afgezet onder verschillende omstandigheden
|
Voorbeeld |
Geleidbaarheid van lithiumionen |
Spanning |
|
LiSiON-80N9 |
4,6 |
~2,0 |
|
LiSiON-100N9 |
7,1 |
~3,9 |
|
LiSiON-120N9 |
2,5 |
~4,2 |
|
LiSiON-100N9A1 |
6,3 |
~5,0 |
|
LiSiON-100N9A5 |
3,0 |
~4,6 |
|
LiSiON-100N5A5 |
2,9 |
~5,2 |
Om de haalbaarheid van het geoptimaliseerde monster LiSiON-100N9A1 voor te verifiëren TFLB-toepassing, MoO3/LiSiON/Li TFLB werd verder vervaardigd. De dwarsdoorsnede FESEM-afbeelding en bijbehorende EDS-afbeeldingen van de MoO3/LiSiON/Li TFLB worden getoond in figuur 4 (a). Als waargenomen, de MoO3-kathode (ongeveer 1,1 µm dik) en de Li-anode zijn goed gescheiden door de LiSiON-elektrolyt, en de LiSiON-elektrolyt heeft dat wel nauwe contactinterfaces met zowel de kathode als de anode. Afb. 4(b) geeft de typische CV-curve van de TFLB weer met een scansnelheid van 0,1 mVâs-1 tussen 1,5-3,5 V, wat een paar goed gedefinieerde redoxpieken vertoont rond 2,25 en 2,65 V, wat overeenkomt met de insertie van lithiumionen in en extractie uit het MoO3[10]. Afb. 4(c) toont de eerste 3 galvanostatische laad-/ontlaadcurven van de TFLB bij a stroomdichtheid van 50 mAâg-1 (20 μAâcm-2, gebaseerd op de massa van MoO3 film). Zoals opgemerkt levert de TFLB resultaten op de initiële laad-/ontlaadcapaciteit van 145/297 mAhâg-1 (58/118,8 μAhâcm-2). Na de 2e cyclus stabiel fietsgedrag met hoge omkeerbaar specifieke capaciteit van 282 mAhâg-1 werd bereikt door de TFLB. De tariefprestaties van de TFLB bij verschillende stroomdichtheden is weergegeven in figuur 4 (d). De onomkeerbaar capaciteitsverlies van de TFLB in de eerste paar cycli bij lage stroomsterkte dichtheid kan worden toegeschreven aan onomkeerbare faseovergang in de afgeleide MoO3 door het inbrengen van lithium[26]. Stabiele ontladingscapaciteiten van ongeveer 219, 173, 107 en 50 mAhâg-1 wordt waargenomen bij respectievelijk 100, 200, 400 en 800 mAâg-1, het aantonen van een goed tariefvermogen. Om de elektrochemische stabiliteit te evalueren van de TFLB werd de cyclusprestatie verder uitgevoerd bij een stroomdichtheid van 200 mAâg-1 (Fig. 4(e)). De TFLB kan na 200 cycli 78,1% van zijn initiële ontladingscapaciteit behouden, en de Coulombische efficiëntie is voor elke cyclus bijna 100%, wat acceptabel blijkt elektrochemische stabiliteit van de LiSiON-elektrolyt. EIS-metingen waren verder uitgevoerd bij nullastspanning om de werking te onderzoeken elektrolyt/elektrode-interface in de TFLB bij verschillende cyclusnummers, en de overeenkomstige Nyquist-plots met equivalent circuit worden weergegeven in figuur 4 (f). Als waargenomen toont de MoO3/LiSiON/Li TFLB een vergelijkbaar EIS-spectrum van twee halve cirkels in het hoge frequentiegebied in de nieuwe staat ten opzichte van die van de MoO3/LiPON/Li TFLB in ons vorige werk[10], wat aangeeft dat de grensvlakweerstand van Li/LiSiON verwaarloosbaar is vergeleken met die van de LiSiON/MoO3-interface[20]. De eerste kleine halve cirkel in de Nyquist-plots is toegeschreven aan de ionische geleiding van Li+-ionen in LiSiON-elektrolyt, terwijl de De tweede grote halve cirkel komt overeen met het ladingsoverdrachtsproces op de LiSiON/MoO3-interface[27,28]. Opgemerkt wordt dat de eerste kleine halve cirkel zelden voorkomt veranderingen tijdens de cycli, wat wijst op de relatief goede cyclische stabiliteit van de LiSiON-elektrolyt. De tweede halve cirkel breidt zich echter geleidelijk uit naarmate de Het cyclusnummer evolueert, waardoor het verhoogde LiSiON/MoO3-grensvlak zichtbaar wordt weerstand tijdens het fietsen, wat de belangrijkste reden voor de capaciteit zou kunnen zijn vervaging van de TFLB[29]. Het is de moeite waard te vermelden dat dit met succes werkt gebruikt de LiSiON-elektrolyt om TFLB te construeren en demonstreert het goede grensvlakcontact van LiSiON met zowel de MoO3-kathode als de lithiumanode voor de eerste keer. Bovendien zijn de grote specifieke capaciteit, goede snelheidsmogelijkheden en aanvaardbare cyclusprestaties van de MoO3/LiSiON/Li TFLB tonen aan dat de LiSiON dunne film is goed toepasbaar als elektrolyt voor TFLB.
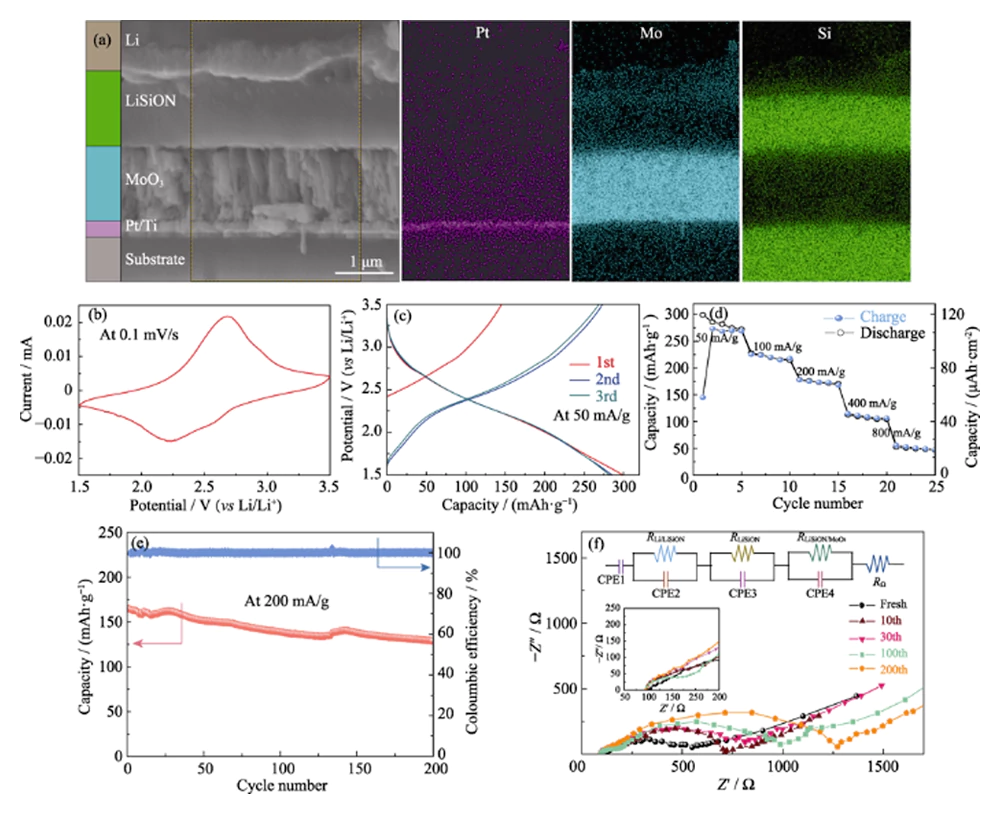
Afb. 4 (a) FESEM-afbeelding in dwarsdoorsnede en bijbehorende EDS-afbeelding afbeeldingen van de MoO3/LiSiON/Li TFLB; (b) Typische CV-curve, (c) initiële drie laad-/ontlaadcurven, (d) snelheid prestaties, (e) cyclusprestaties en (f) EIS-spectra bij verschillende cycli nummers van de MoO3/LiSiON/Li TFLB met monster LiSiON-100N9A1 als elektrolyt
3 conclusies
Samenvattend was amorfe LiSiON dunnefilm-elektrolyt met succes bereid door RF-magnetronsputteren met behulp van Li2SiO3-doelwit met N2/Ar-gasstroom. De geoptimaliseerde dunne LiSiON-film wordt afgezet onder een RF-vermogen van 100 W bij de stroom van 90 sccm N2 en 10 sccm Ar hebben een glad oppervlak, een dichte structuur en een hoog ionengehalte geleidbaarheid (6,3×10-6 Sâcm-1) en een breed spanningsvenster (5 V), waardoor het een veelbelovende elektrolytmateriaal voor TFLB. Belangrijker nog: door gebruik te maken van de LiSiON elektrolyt werd met succes een MoO3/LiSiON/Li TFLB gedemonstreerd voor de eerste keer met hoge specifieke capaciteit (282 mAhâg-1 bij 50 mAâg-1), goede snelheidsprestaties (50 mAhâg-1 bij 800 mAâg-1), en aanvaardbare cyclusstabiliteit (78,1% capaciteitsbehoud na 200 cycli). Verwacht wordt dat dit werk nieuwe kansen zal opleveren voor de ontwikkeling van hoogwaardige prestatie TFLB door gebruik te maken van op Li2O-SiO2 gebaseerde dunnefilm-elektrolyt.
Referenties
[1] MOITZHEIM S, PUT B, VEREECKEN P M. Vooruitgang op het gebied van 3D dunne-film Li-ionbatterijen. Interfaces voor geavanceerde materialen, 2019,6(15):1900805.
[2] XIA Q, ZHANG Q, SUN S, et al. Tunnelvergroeiing LixMnO2-nanobladarrays als 3D-kathode voor hoogwaardige, volledig vaste-stof dunne-film lithiummicrobatterijen. Geavanceerde materialen, 2021,33(5):2003524.
[3] DENG Y, EAMES C, FLEUTOT B, et al. Verbetering van de geleidbaarheid van lithiumionen in vaste elektrolyten van lithiumsuperionische geleider (LISICON) door een gemengd polyanioneffect. ACS toegepaste materialen en interfaces, 2017,9(8):7050-7058.
[4] BATES JB, DUDNEY NJ, GRUZALSKI GR, et al. Fabricage en karakterisering van dunne films van amorfe lithiumelektrolyt en oplaadbare dunnefilmbatterijen. Journal of Power Sources, 1993,43(1/2/3):103-110.
[5] BATES J. Elektrische eigenschappen van dunne films van amorfe lithiumelektrolyt. Solid State Ionics, 1992,53(56):647-654.
[6] FAMPRIKIS T, GALIPAUD J, CLEMENS O, et al. Samenstellingsafhankelijkheid van ionische geleidbaarheid in LiSiPO (N) dunnefilmelektrolyten voor vastestofbatterijen. ACS toegepaste energiematerialen, 2019,2(7):4782-4791.
[7] DENG Y, EAMES C, CHOTARD JN, et al. Structurele en mechanistische inzichten in snelle lithium-iongeleiding in Li4SiO4-Li3PO4 vaste elektrolyten. Tijdschrift van de American Chemical Society, 2015,137(28):9136-9145.
[8] CHEN R, SONG X. De ionische geleidbaarheid van vaste elektrolyten voor Li4+xMxSi1-xO4-yLi2O (M=Al, B) systemen. Tijdschrift van de Chinese Chemical Society, 2002, 49: 7-10.
[9] ADNAN S, MOHAMED N S. Effecten van Sn-substitutie op de eigenschappen van Li4SiO4 keramische elektrolyt. Ionics in vaste toestand, 2014,262:559-562.
[10] SUN S, XIA Q, LIU J, et al. Op zichzelf staande zuurstofarme α-MoO3-x nanoflake-arrays als 3D-kathode voor geavanceerde, volledig vaste-stof dunne-film-lithiumbatterijen. Journal of Materiomics, 2019,5(2):229-236.
[11] DING W, LU W, DENG X, et al. Een XPS-onderzoek naar de structuur van SiNx-film afgezet door microgolf-ECR-magnetronsputteren. Acta Physica Sinica, 2009,58(6):4109-4116.
[12] KIM H, KIM Y. Gedeeltelijke nitridatie van Li4SiO4 en ionische geleidbaarheid van Li4. 1SiO3. 9N0. 1Ceramics International, 2018,44(8):9058-9062.
[13] MARIKO M, HIDEMASA K, TOMOYUKI O, et al. Analyse van SiO-anodes voor lithium-ionbatterijen. Publicatieblad van de Electrochemical Society, 2005,152(10):A2089.
[14] FINGERLE M, BUCHHEIT R, SICOLO S, et al. Reactie- en ruimteladingslaagvorming op het LiCoO2-LiPON-grensvlak: inzichten in defectvorming en uitlijning van ionenenergieniveaus door een gecombineerde oppervlaktewetenschap-simulatiebenadering. Chemische materialen, 2017,29(18):7675-7685.
[15] WEST W, HOOD Z, ADHIKARI S, et al. Vermindering van de weerstand tegen ladingsoverdracht aan het grensvlak van vaste elektrolyt en elektrode door gepulseerde laserafzetting van films uit een kristallijne Li2PO2N-bron. Journal of Power Sources, 2016,312:116-122.
[16] SICOLO S, FINGERLE M, HAUBRAND R, et al. Grensvlakinstabiliteit van amorfe LiPON tegen lithium: een gecombineerde dichtheidsfunctionaaltheorie en spectroscopisch onderzoek. Journal of Power Sources, 2017,354:124-133.
[17] WU F, LIU Y, CHEN R, et al. Bereiding en prestatie van nieuwe Li-Ti-Si-P-O-N dunne-film elektrolyt voor dunne-film lithiumbatterijen. Journal of Power Sources, 2009,189(1):467-470.
[18] PUT B, VEREECKEN M, MEERSSCHAUT J, et al. Elektrische karakterisering van ultradunne RF-gesputterde LiPON-lagen voor batterijen op nanoschaal. ACS toegepaste materialen en interfaces, 2016,8(11):7060-7069.
[19] NIINOMI H, MOTOYAMA M, IRIYAMA Y. Li+ Geleiding in Li-Nb-O-films afgezet met een Sol-Gel-methode. Ionics in vaste toestand, 2016,285:13-18.
[20] SONG S, LEE K, PARK H. Hoogwaardige, flexibele, volledig vaste microbatterijen op basis van vaste elektrolyt van lithiumbooroxynitride. Journal of Power Sources, 2016,328:311-317.
[21] OHTSUKA H, OKADA S, YAMAKI J. Solid state batterij met Li2O-V2O5-SiO2 vaste elektrolyt dunne film. Ionics in vaste toestand, 1990, 40-41: 964-966.
[22] Kalita D, Lee S, Lee K, et al. Ionische geleidbaarheidseigenschappen van amorfe Li-La-Zr-O vaste elektrolyt voor dunne-filmbatterijen. Ionics in vaste toestand, 2012,229:14-19.
[23] SAKURAI Y, SAKUDA A, HAYASHI A, et al. Bereiding van amorfe Li4SiO4-Li3PO4 dunne films door gepulseerde laserafzetting voor secundaire lithiumbatterijen met volledige vaste stof. Ionics in vaste toestand, 2011,182:59-63.
[24] TANG, WU F, LI L, et al. Magnetronsputterpreparaat van op stikstof opgenomen dunnefilmelektrolyten op basis van lithium-aluminium-titaanfosfaat voor volledig vaste lithiumionbatterijen. Het Journal of Physical Chemistry C, 2012,116(5):3817-3826.
[25] YU X, BATES JB, JELLISON G, et al. Een stabiele dunnefilm-lithiumelektrolyt: lithiumfosforoxynitride. Publicatieblad van de Electrochemical Society, 1997,144(2):524.
[26] KIM H, COOK J, LIN H, et al. Zuurstofvacatures verbeteren de pseudocapacitieve ladingsopslageigenschappen van MoO3-x. Natuurmaterialen, 2017,16:454-460.
[27] SONG H, WANG S, SONG X, et al. Volledig op zonne-energie werkende lithium-luchtbatterijen die werken bij extreem lage temperaturen. Energie- en milieuwetenschappen, 2020,13(4):1205-1211.
[28] WANG Z, LEE J, XIN H, et al. Effecten van de kathode-elektrolyt-grensvlaklaag (CEI) op de lange termijncyclus van volledig vaste dunne-filmbatterijen. Journal of Power Sources, 2016,324:342-348.
[29] QIAO Y, DENG H, HE P, et al. Een lithium-metaalcel van 500 Wh/kg op basis van anionische redox. Joule, 2020,4(6):1311-1323.



