Categorieën
nieuwe blog
- Handleiding voor de selectie van batterij-elektrolyten: wat inkoopmanagers moeten weten
- Apparatuur voor knoopcelbatterijlaboratoria: de complete checklist voor R&D-laboratoria voor batterijen
- Vergelijking van kathodematerialen voor batterijen: NMC, LFP en NCA
- Trends in de productie van lithium-ionbatterijen tot 2026: een B2B-kopersgids
- Stapsgewijze handleiding voor het productieproces van lithium-ionbatterijen
Tags
F-gedoteerde koolstofgecoate nano-Si-anode met hoge capaciteit
F-gedoteerde koolstofcoating Nano-Si-anode met hoge capaciteit: voorbereiding door gasvormige fluorering en Prestaties voor lithiumopslag
Auteur: SU Nan, QIU Jieshan, WANG Zhiyu. F-gedoteerd Met koolstof gecoate nano-Si-anode met hoge capaciteit: voorbereiding door gasvormige fluorering en prestaties voor lithiumopslag. Journal of Anorganische Materialen, 2023, 38(8): 947-953 DOI:10.15541/jim20230009
Samenvatting
Si-anodes hebben een enorm potentieel bij de ontwikkeling van hoogenergetische Li-ion batterijen. Maar snel falen als gevolg van enorme volumeveranderingen bij Li-opname belemmert hun toepassing. Dit werk rapporteert een gemakkelijke maar laag-giftige gasfluorering manier om F-gedoteerde koolstofgecoate nano-Si-anodematerialen te verkrijgen. Coating van nano-Si met F-gedoteerde koolstof die hoge defecten bevat, kan Si effectief beschermen van enorme volumeveranderingen bij Li-opslag terwijl Li+-transport wordt gefaciliteerd vorming van stabiele LiF-rijke vaste elektrolyt-interfase (SEI). Deze anode vertoont hoge capaciteiten van 1540-580 mAh·g-1 bij diverse huidige tarieven van 0,2-5,0 A·g-1, met behoud van 75% capaciteit na 200 cycli. Deze methode richt zich ook op de problemen van hoge kosten en toxiciteit van traditionele fluoreringstechnieken waarbij fluor wordt gebruikt bronnen zoals XeF2 en F2.
Zoekwoordenï¼ Li-ionbatterij; Si-anode; F-gedoteerde koolstof; gasvormige fluorering methode
Het ontwikkelen van efficiënte energieopslag en conversietechnologieën zullen helpen het doel van koolstofpiek te bereiken koolstofneutraliteitâ. Lithium-ionbatterijen zijn momenteel een van de meest gebruikte gebruikte hoogefficiënte technologieën voor energieopslag [1]. Commercieel echter Grafietanodes hebben een lage lithiumopslagcapaciteit, wat de opslagcapaciteit aanzienlijk beperkt energiedichtheid van lithium-ionbatterijen [2]. Silicium heeft de voordelen van laag potentiële en overvloedige reserves, en de theoretische specifieke capaciteit ervan (4200 mAh·g-1) is veel hoger dan die van grafietanode, dus wordt het beschouwd als een kandidaat-anodemateriaal ter vervanging van grafiet [3]. Siliciummaterialen bereiken dit lithiumopslag op basis van de omkeerbare legeringsreactie met lithiumionen, maar dit proces gaat gepaard met enorme volumeveranderingen (~400%), wat leidt tot snelle verpoedering en falen van de elektrode, wat een belangrijk knelpunt wordt beperking van de praktische toepassing van siliciumanodes [3-4].
De afgelopen jaren hebben onderzoekers dat gedaan ontwikkelde een verscheidenheid aan strategieën om de stabiliteit en elektrochemie te verbeteren prestaties van siliciumanodes. Zoals: nanometerisering [5], structureel composiet met geleidende koolstof en andere materialen [6-7], enz. Verbeter de structurele stabiliteit van de siliciumanode door het verlichten van de mechanische spanning geassocieerd met de volume-uitbreiding van de lithiumopslag op microscopisch niveau schaal. Ontwikkel nieuwe elektrolyten of elektrolytadditieven om de stabiliteit en Coulomb-efficiëntie van de grensvlakfase van vaste elektrolyten (SEI) op het oppervlak van de siliciumanode [8]. Ontwikkel efficiënt polymeer bindmiddelen (zoals natriumcarboxymethylcellulose, natriumalginaat, polyacryl zuurgebaseerd polyrotaxaan [9], enz.). Versterk de verbindende kracht tussen actief materialen, tussen actieve materialen en geleidend netwerk, en tussen elektrodefilm en stroomcollector [9-10]. Onder hen is koolstofcoating er één van de meest effectieve manier om de structurele stabiliteit van siliciumanodes te verbeteren en moduleer oppervlakte- en interface-eigenschappen [3-4,11]. Echter, de strak gecoate zeer stabiele koolstoflaag belemmert ook het transport en beperkingen van lithiumionen de volledige prestaties van de siliciumanode.
Daarnaast het herhaalde volume veranderingen van de siliciumanode tijdens het continue laad- en ontlaadproces zorgen er ook voor dat de SEI-film voortdurend breekt en herhaaldelijk groeit, wat resulteert in het voortdurende verlies van actief lithium en elektrolyt op het elektrodeoppervlak [12]. Als antwoord op de bovenstaande problemen stelt deze studie een efficiënte oplossing voor gasfasefluoreringsmethode om het oppervlak van het siliciumanodemateriaal te coaten met een zeer defecte amorfe koolstoflaag die rijk is aan fluorelementen verbetering van de structuur en interfacestabiliteit. Vergeleken met traditioneel fluoreringstechnologie die gebruik maakt van dure en zeer giftige fluorbronnen zoals XeF2 of F2 [13], deze strategie is eenvoudiger en minder giftig. De Met fluor gedoteerde koolstoflaag die het oppervlak van nano-siliciummaterialen bedekt, kan dat wel effectief bufferen van de volume-uitbreiding van in lithium ingebedde siliciumanodes terwijl het transportvermogen van lithiumionen wordt verbeterd. En een zeer stabiele SEI film rijk aan anorganisch fluoride wordt in situ geconstrueerd om het doel te bereiken verbetering van de cyclusstabiliteit van de siliciumanode.
1 Experimentele methode
1.1 Materiaalvoorbereiding
Preparaat van koolstofcoating nanosilicium (Si@C): 0,3 g commercieel nanosilica poeder (deeltjesgrootte 20 ~ 100 nm, Aladdin's reagens) werd ultrasoon gemaakt gedispergeerd in 28 ml van een gemengd oplosmiddel van gedeïoniseerd water en ethanol (volume verhouding 5:2). Roer na het toevoegen van 0,4 ml 3-aminopropyltriethoxysilaan gedurende 2 uur om een uniforme dispersie te vormen A. Los 0,115 g 4,4-dihydroxydifenyl op sulfide en 0,1 g 3-aminofenol in 28 ml van een gemengd oplosmiddel van gedeïoniseerd water en ethanol (volumeverhouding 5:2) om een homogene oplossing te vormen. B. Mengen dispersie A en oplossing B gelijkmatig verdelen, 0,1 ml ammoniakwater toevoegen, 30 minuten roeren, Voeg vervolgens 0,14 ml formaldehyde-oplossing (37%~40%) toe en laat reageren met constant roeren bij 30 °C gedurende 12 uur. Na de reactie wordt de fenolhars bekleed nanosilica (Si@AF) werd verkregen door centrifugeren en wassen met ethanol en gedeïoniseerd water afwisselend driemaal. Het werd gecalcineerd in argongas bij 800 °C gedurende 3 uur om met koolstof gecoat nanosilicium (Si@C) te verkrijgen.
Bereiding van met fluor gedoteerd met koolstof gecoat nanosilicium (Si@C-F): 100 mg Si@C en 200 mg polyvinylideenfluoride (PVDF) werden in een met argon beschermde buisoven geplaatst. De kwartsboot met PVDF bevindt zich stroomopwaarts van de luchtstroom en de kwartsboot met Si@C bevindt zich stroomafwaarts van de luchtstroom. Het is geroosterd bij 600 °C gedurende 3 uur om met fluor gedoteerde, met koolstof gecoate nano-silicium (Si@C-F) te verkrijgen.
1.2 Batterijassemblage en testen van elektrochemische prestaties
1.2.1 Batterijmontage
Monteer de CR2016-knoopcelbatterij voor testen. Meng het actieve materiaal, geleidend carbonzwart en carboxymethylcellulose-natriumbindmiddel gelijkmatig in een massaverhouding van 7:2:1. Gedeïoniseerd water werd toegevoegd als oplosmiddel en dispergeermiddel, en de verkregen slurry werd verkregen gelijkmatig gecoat op de koperfolie als werkelektrode. Het actieve materiaal de belasting bedroeg 0,8~1,0 mg·cm-2. Als toonbank werden metalen lithiumplaten gebruikt elektroden en referentie-elektroden. De elektrolyt is een DOL/DME-oplossing opgelost in 1,0 mol/l LiTFSI (lithiumbistrifluormethaansulfonaatimide) en 2,0% LiNO3 (DOL is 1, 3-dioxolaan, DME is ethyleenglycol-dimethylether, volume verhouding 1:1). Monteer de cel in een met argon gevulde handschoenenkast (watergehalte < 0,1 μL/L, zuurstofgehalte < 0,1 μL/L).
1.2.2 Batterijprestatietest
Gebruik de IVIUM Vertex.C.EIS elektrochemische stof werkstation om het reactiemechanisme en de reactiekinetiek van de batterij met behulp van de Cyclische Voltammetrie (CV)-methode. Het spanningsbereik is 0,01~1,5 V, en de sweepsnelheid is 0,05~0,5 mV·s- 1. Elektrochemische impedantie Spectroscopie (EIS) werd gebruikt om de elektrodedynamiek te analyseren. De testfrequentie het bereik was 100 kHz ~ 10 mHz en de amplitude van de verstoringsspanning was 5,0 mV. Land CT2001A batterijtester werd gebruikt om de prestaties van lithiumopslag te bestuderen met behulp van de constante stroomlaad- en ontlaadmethode. Het spanningsvenster was 0,01~1,5 V (vs. Li/Li+), en de stroomdichtheid was 0,2~5,0 A·g-1.
2 Resultaten en discussie
2.1 Analyse van uiterlijk, structuur en samenstelling van materialen
Het voorbereidingsproces van Met fluor gedoteerde, met koolstof gecoate nano-siliciummaterialen worden getoond in Figuur 1. Eerst worden met polymeer beklede siliciumnanodeeltjes (Si@AF) vervaardigd op basis van fenol-aldehyde condensatie polymerisatiereactie en omgezet in amorfe, met koolstof beklede nano-silicium nanodeeltjes (Si@C) bij hoge temperatuur. Dan polyvinylideenfluoride wordt gebruikt als fluorbron en fluor wordt gedoteerd via de gasfase in de koolstoflaag buiten de siliciumnanodeeltjes fluoreringsmethode bij hoge temperatuur. Figuur 2(a) toont de XRD-patronen van Si@C- en Si@C-F-materialen. Diffractiepieken gelegen op 2θ=28°, 47°, 56°, 69° en 76°. Ze komen overeen met het kristal (111), (220), (311), (400) en (331). vlakken van respectievelijk monokristallijn silicium (JCPDS 77-2108). De brede piek gelegen bij 2θ=25°~26° wordt toegeschreven aan de gevormde koolstofstructuur op korte afstand door de carbonisatie van het fenolische condensatiepolymerisatieproduct. De koolstofcoatinglaag met hoge geleidbaarheid en uitstekende structurele flexibiliteit kan het verpulveringsfalen van siliciummaterialen effectief verlichten tijdens het laad- en ontlaadproces en verbeter de geleidbaarheid van de elektrode. Figuur 2(b) is het Raman-spectrum van Si@C- en Si@C-F-materialen, met voor de hand liggende absorptiepieken verschijnen bij 515, 947, 1350 en 1594 cm-1. Onder hen de absorptiepieken bij 515 en 947 cm-1 zijn de karakteristieke pieken van kristallijn silicium, die zijn afgeleid van het fotofonon van de eerste orde verstrooiing en de transversale fotofononverstrooiing van de tweede orde van silicium respectievelijk [14]. De absorptiepieken bij 1350 en 1594 cm-1 komen overeen met de aromatische koolstofconfiguratie die trillingen uitbreidt (G-modus) en het ongeordende defecte koolstofstructuur (D-modus), respectievelijk. Over het algemeen gesproken is de intensiteitsverhouding van D-modus en G-modus (ID/IG) kan worden gebruikt om de mate te meten van defecten en wanorde van koolstofmaterialen [15]. Vergeleken met Si@C-materiaal (ID/IG=0,99) neemt de ID/IG van Si@C-F-materiaal toe tot 1,08. Het laat zien dat de Het fluoreringsproces kan de defecten van de koolstofcoatinglaag vergroten, wat gunstig is voor het strak coaten van nano-silicium en tegelijkertijd het lithiumion verbetert transportmogelijkheden.
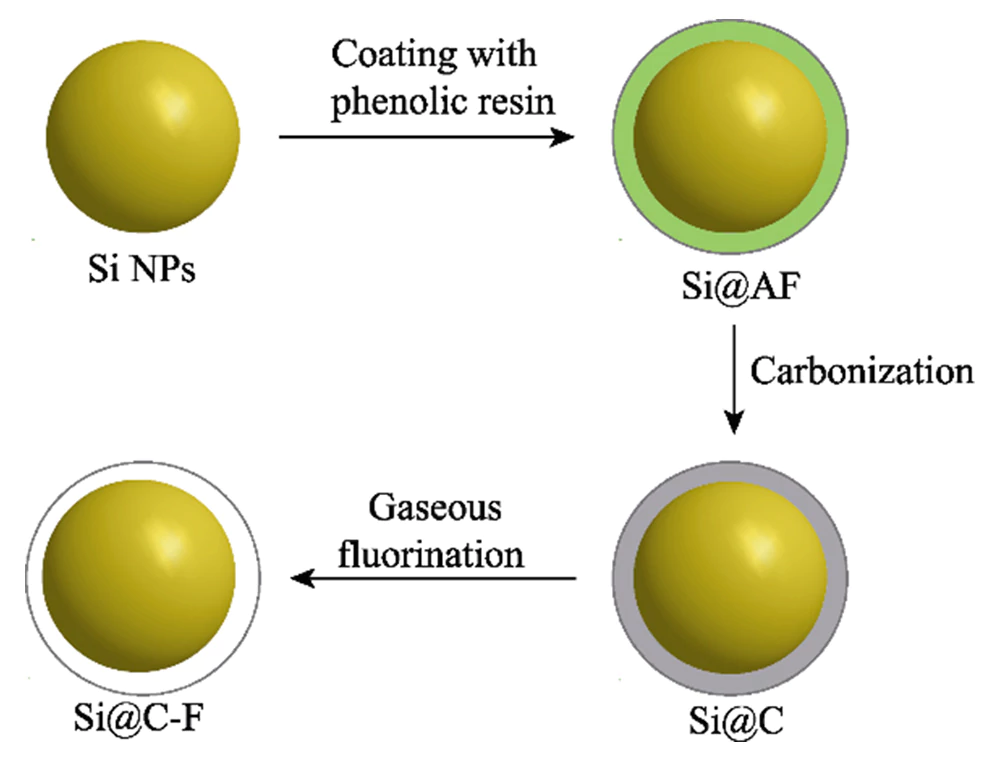
Afb. 1 Schematische weergave van de productie van Si@C-F
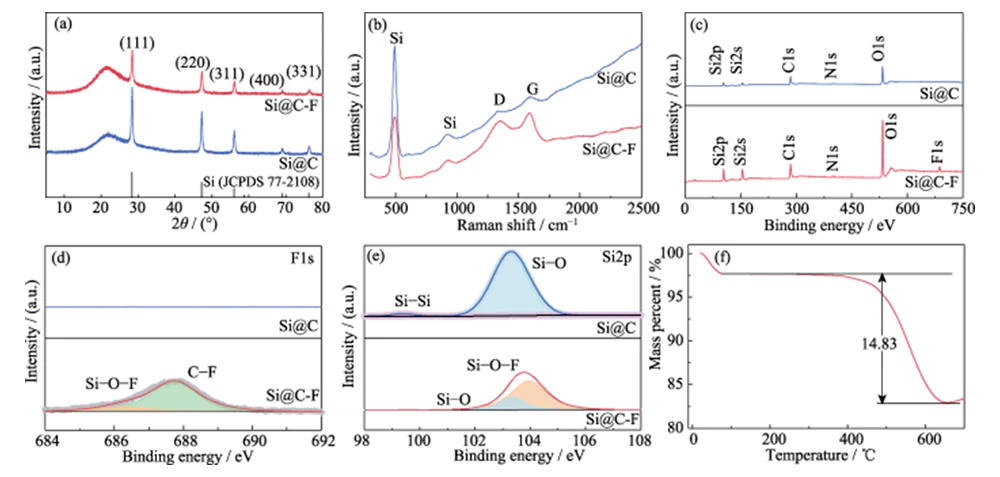
Afb. 2 (a) XRD-patronen, (b) Raman-spectra, (c) XPS onderzoeksscan, (d) F1's met hoge resolutie en (e) Si2p XPS-spectra van Si@C en Si@C-F, (f) TGA-curve van Si@C-F
Het volledige XPS-spectrum laat zien dat de Si@C-materiaal bevat O-, N-, C- en Si-elementen (Figuur 2 (c)). Het atomaire fractie van het F-element in het Si@C-F-materiaal verkregen na fluorering behandeling bedraagt ongeveer 1,8%. In het F1s XPS-spectrum met hoge resolutie (Figuur 2(d)), de twee karakteristieke pieken bij de bindingsenergie van 686,3 en 687,8 eV komt respectievelijk overeen met C-F en Si-O-F, en C-F is de dominante een. Het laat zien dat de fluoreringsbehandeling met succes fluor introduceerde element in de amorfe koolstoflaag die op het oppervlak van nano-silicium is gecoat. De hoge resolutie Si2p (Figuur 2(e)) en F1s XPS-spectra bewijzen dat Si-atomen chemisch interageren met het F-element in de koolstoflaag door Si-O-F te vormen bindingen, wat gunstig is voor de strakke coating van de koolstoflaag op de silicium oppervlak. Thermogravimetrische analyse (TGA) laat zien dat de massafractie van Si in het Si@C-F-materiaal is ongeveer 85,17% (Figuur 2(f)).
SEM-analyse laat zien dat de Si@C-F materiaal bestaat uit nanodeeltjes met een grootte van <100 nm (Figuur 3(a~c)). Na carbonisatie bij hoge temperatuur en fluorering in de gasfase wordt het koolstofmateriaal nog steeds gelijkmatig op het oppervlak van de siliciumnanodeeltjes gecoat.
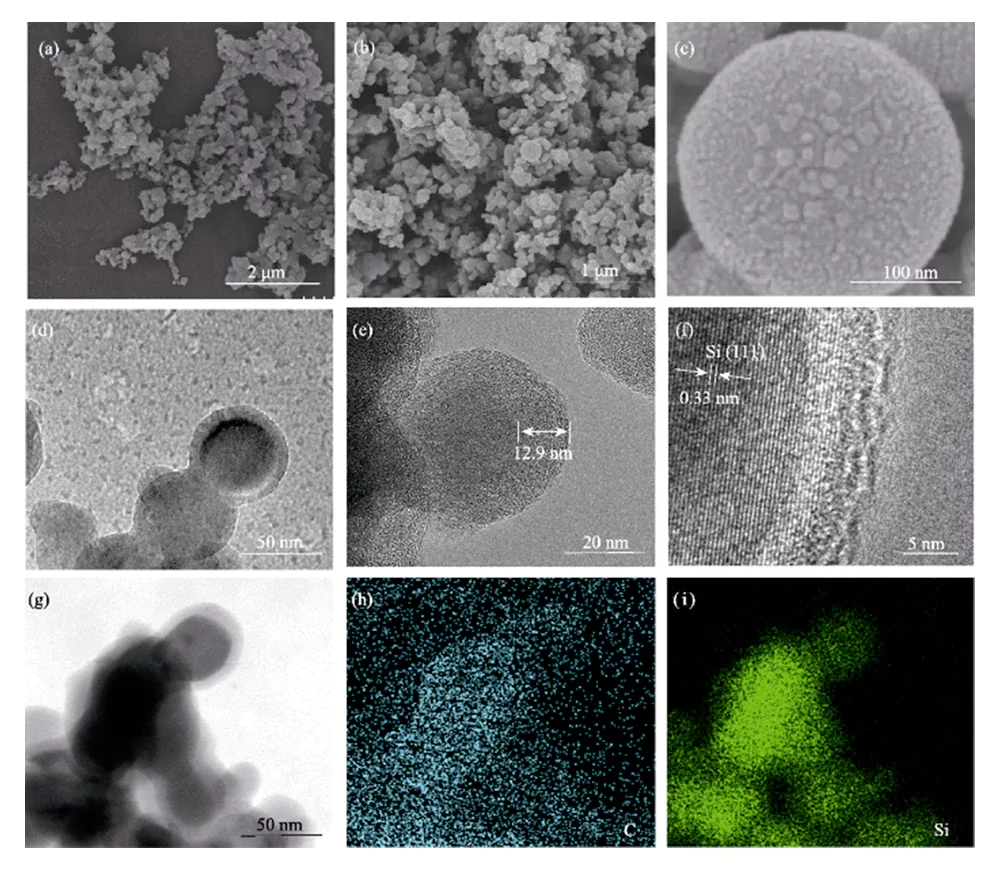
Afb. 3 (a-c) SEM-afbeeldingen, (d-f) TEM-afbeeldingen en (g-i) elementaire afbeelding van Si@C-F
TEM-analyse toont aan dat het silicium nanodeeltjes zijn volledig en gelijkmatig bedekt met een koolstoflaag met een dikte van ongeveer tien nanometer, waardoor een kern-schilstructuur ontstaat (Figuur 3(d~e)). Siliciumnanodeeltjes hebben een enkele kristalstructuur, waarin de roosterafstand van 0,328 nm komt overeen met het (111) kristalvlak van Si, en de met fluor gedoteerde koolstoflaag die deze bedekt, heeft een amorfe structuur (Figuur 3(f)). Het elementverdelingsspectrum bewijst dat C- en Si-elementen dat wel zijn gelijkmatig verdeeld in Si@C-F (Figuur 3(g~i)).
2.2 Elektrochemische eigenschappen van materialen
Figuur 4(a, b) is de CV-curve van Si@C- en Si@C-F-anodematerialen. De sweepsnelheid is 0,1 mV·s-1 en het spanningsbereik is 0,01~1,5 V. In de eerste cyclus komt de zwakke brede piek in het bereik van 0,1 ~ 0,4 V overeen met de onomkeerbaar proces van ontleding van elektrolyten om een SEI-film te vormen; de reductiepiek bij 0,01 V komt overeen met het proces van kristallijn silicium vorming van silicium-lithiumlegering (LixSi) door middel van een legeringsreactie. Tijdens de daaropvolgende laadproces komen de twee oxidatiepieken bij 0,32 en 0,49 V overeen met de proces van het dealloyeren van LixSi om amorf silicium te vormen [16]. Fluorering behandeling kan structurele doping- en etseffecten bewerkstelligen. Een groot aantal structurele defecten worden geïntroduceerd in de amorfe koolstoflaag die erop is aangebracht oppervlak van het Si-materiaal om een driedimensionaal lithiumionentransport te vormen kanaal, versnel het transport van lithiumionen en verbeter de elektrochemische stof reactiviteit van het Si-materiaal. Daarom vertoont Si@C-F een scherpere delithiatie-oxidatiepiek bij 0,49 V dan de Si@C-anode zonder fluor doping. Tijdens het daaropvolgende ontladingsproces bedraagt de nieuwe reductiepiek 0,19 V komt overeen met het lithium-insertieproces van gevormd amorf silicium tijdens het eerste laadproces [16-17]. Naarmate het aantal cycli toeneemt, de posities van de oxidatiepiek en de reductiepiek in de CV-curve nr langere verandering, wat aangeeft dat Si@C en Si@C-F anodematerialen een soortgelijk patroon volgen legeringslithiumopslagmechanisme na de eerste lading en ontlading. Tijdens Bij dit proces namen de oxidatiepiek en de reductiepiek geleidelijk toe, weerspiegelt een typisch elektrode-activatieproces.
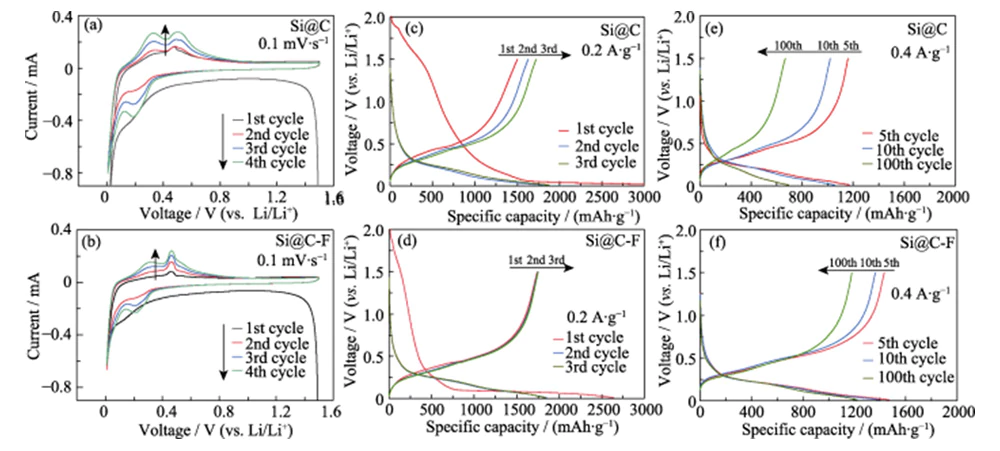
Afb. 4 (a, b) CV-curven bij een scansnelheid van 0,1 mV·s-1 en laad-ontlaadspanningscurven bij (c, d) 0,2 en (e, f) 0,4 A·g-1 voor (a, c, e) Si@C en (b, d, f) Si@C-F anodes
In de constante stroomlading en ontladingstest, het Si-anodemateriaal werd 4 keer in cyclus gebracht en geactiveerd bij a lagere stroomdichtheid (0,2 A·g-1), en vervolgens werd de cyclusstabiliteit ervan getest bij a stroomdichtheid van 0,4 A·g-1. Figuur 4 (c, d) toont de galvanostatische lading en ontladingscurven van Si@C- en Si@C-F-anodes bij 0,2 A·g-1, en de spanning venster is 0,01 ~ 1,5 V. Tijdens het eerste ontladingsproces vormden beide een lange platform in het spanningsbereik <0,1 V, overeenkomend met het lithiuminvoegproces van kristallijne siliciumlegeringen. Dit proces gaat vaak gepaard met een laag eerste Coulomb-rendement. Tijdens het eerste oplaadproces wordt de silicium-lithiumlegering gedelithieerd en getransformeerd in amorf silicium met een lagere activeringsenergie voor het inbrengen van lithium [18], waardoor het potentieel voor het inbrengen van lithium toeneemt tot 0,1 ~ 0,3 V na het eerste opladen en ontladen. Vergeleken met Si@C is de specifieke capaciteit voor de eerste ontlading (2640 mAh·g-1) van de Si@C-F-anode iets lager. De eerste ladingsspecifieke capaciteit (1739,6 mAh·g-1) is echter hoger, en de eerste Coulombische efficiëntie (65,9%) is ongeveer 45,8% hoger dan die van de Si@C-anode. De lading-ontladingscurve van het SEI-gebied van de Si@C-F negatieve elektrode is korter dan die van Si@C, wat aangeeft dat er een stabielere SEI-film op het oppervlak wordt gevormd. Dit komt omdat de met fluor gedoteerde koolstoflaag bevorderlijk is voor het induceren van de vorming van een SEI-film die anorganische componenten (zoals LiF) bevat en een hogere stabiliteit op het oppervlak van de siliciumanode, waardoor onomkeerbaar lithiumverlies en elektrolytverbruik worden verminderd [19].
Figuur 4(e~f) toont de laad- en ontlaadcurven van Si@C en Si@C-F negatieve elektroden met een stroomdichtheid van 0,4 A·g-1 na activering. Na 100 cycli kan de Si@C-F-anode nog steeds een hoge specifieke capaciteit behouden van 1223 mAh·g-1, met een capaciteitsbehoud van 85% (Figuur 5(a)). Onder onder dezelfde omstandigheden, de capaciteit van de Si@C negatieve elektrode zonder fluoreringsbehandeling verviel snel tijdens het laad- en ontlaadproces, en het capaciteitsbehoud na 100 cycli was slechts 62%. Dat blijkt de met fluor gedoteerde koolstofcoatinglaag heeft een aanzienlijk effect op de verbetering de cyclusstabiliteit van de siliciumanode. Commercieel nano-siliciumanodes zonder koolstofcoating zullen na meer dan 10 cycli kapot gaan als gevolg van enorme volume-uitbreiding en structurele verpoedering tijdens de deintercalatie van lithium. Tijdens dit proces wordt de specifieke capaciteit van Si@C-F en Si@C negatieve elektroden nemen geleidelijk toe in de eerste 10 tot 20 cycli vanwege het activeringseffect. Bij een grote stroomdichtheid van 0,2 ~ 5,0 A·g-1, de Si@C-F-anode kan een hoge specifieke capaciteit van 1540~580 handhaven mAh·g-1, met uitstekend capaciteitsbehoud (Figuur 5(b)). Bij hoge stroom dichtheid van 5,0 A·g-1, is het capaciteitsbehoud ongeveer 78% hoger dan die van Si@C. Wanneer de stroomdichtheid verder wordt verlaagd tot 0,2 A·g-1, de specifieke capaciteit kan worden hersteld tot 1450 mAh · g-1, wat aangeeft dat dit het geval is structuur is zeer stabiel tijdens lithiumopslag met hoge snelheid. Na 200 laad-ontlaadcycli bij een stroomdichtheid van 0,2 A·g-1 kan de Si@C-F-anode een specifieke capaciteit van 75% behouden. Het capaciteitsbehoudpercentage van de De Si@C-anode zonder fluoreringsbehandeling bedraagt slechts 40% (Figuur 5(c)). Deze anode vertoont ook betere lithiumopslagprestaties dan het siliciumanodemateriaal gerapporteerd in de literatuur (Tabel 1).
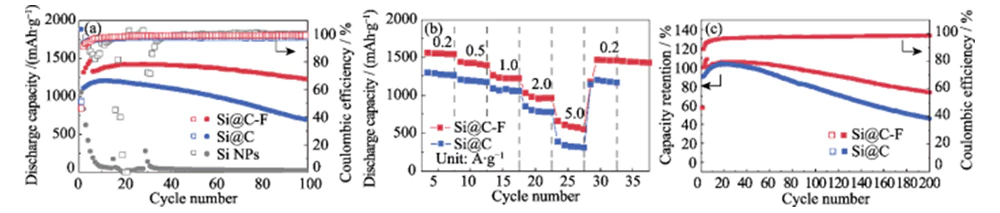
Afb. 5 (a) Fietsstabiliteit bij een stroomdichtheid van 0,4 A·g-1 met anodes geactiveerd door 4 cycli bij 0,2 A·g-1 vóór het fietsen, en (b) snelheidsvermogen bij verschillende stroomdichtheden variërend van 0,2 tot 5,0 A·gâ1 en (c) capaciteitsbehoud bij een stroomdichtheid van 0,2 A·g-1 voor lithiumopslag in Si@C- en Si@C-F-anode
Tabel 1 Vergelijking van Si@C-F-anode met gerapporteerde Si-gebaseerde anode in elektrochemische prestaties
|
Materialen |
Initiële CE |
Initiële capaciteit/(mAh·g-1) |
Capaciteit rbehoud |
Referentie |
|
Si@C-F |
65,9% |
2640 |
85% (100 cycli) |
Dit werk |
|
nano-Si/TiN@ |
71% |
2716 |
59,4% (110 cycli) |
[20] |
|
Si@C@RGO |
74,5% |
1474 |
48,9% (40 cycli) |
[21] |
|
Si@FA |
65% |
1334 |
68,7% (100 cycli) |
[22] |
|
p-Si@C |
58% |
3460 |
57,5% (100 cycli) |
[23] |
|
Si@void@C |
- |
900 |
70% (100 cycli) |
[24] |
|
Si/C@C |
- |
1120 |
80% (100 cycli) |
[25] |
Bij hoge stroom dichtheid van 5,0 A·g-1, is het capaciteitsbehoud ongeveer 78% hoger dan die van Si@C. Wanneer de stroomdichtheid verder wordt verlaagd tot 0,2 A·g-1, de specifieke capaciteit kan worden hersteld tot 1450 mAh · g-1, wat aangeeft dat dit het geval is structuur is zeer stabiel tijdens lithiumopslag met hoge snelheid. Na 200 laad-ontlaadcycli bij een stroomdichtheid van 0,2 A·g-1 kan de Si@C-F-anode een specifieke capaciteit van 75% behouden. Het capaciteitsbehoudpercentage van de De Si@C-anode zonder fluoreringsbehandeling bedraagt slechts 40% (Figuur 5(c)). Deze anode vertoont ook betere lithiumopslagprestaties dan het siliciumanodemateriaal gerapporteerd in de literatuur (Tabel 1). De hoeveelheid fluordotering in de coating koolstoflaag heeft een aanzienlijke invloed op de lithiumopslagprestaties van de Si@C-F-anode. Wanneer de hoeveelheid fluordotering lager is dan 1,8% atomaire fractie, de cyclusstabiliteit van de Si@C-F-anode verbetert aanzienlijk naarmate de De hoeveelheid fluordoping neemt toe (Figuur 6). Dit komt door het versterkte effect van fluordotering op de lithiumiontransporteigenschappen van de koolstof coatinglaag en de stabiliteit van de SEI-film op het oppervlak van het silicium materiaal. Wanneer de fluordoteringsverhouding te hoog is (2,7%), kan de koolstofgecoat Si-anodemateriaal behoudt nog steeds een goede cyclusstabiliteit, maar de de specifieke capaciteit neemt aanzienlijk af. Dit komt door het verlies van actief Si veroorzaakt door etsen van fluorsoorten in de gasfase tijdens hoge temperaturen fluorering. Wanneer de fluordoteringshoeveelheid 1,8 atoomprocent bedraagt, wordt de Si@C-F anode vertoont optimale cyclusstabiliteit en hoge specifieke capaciteit.
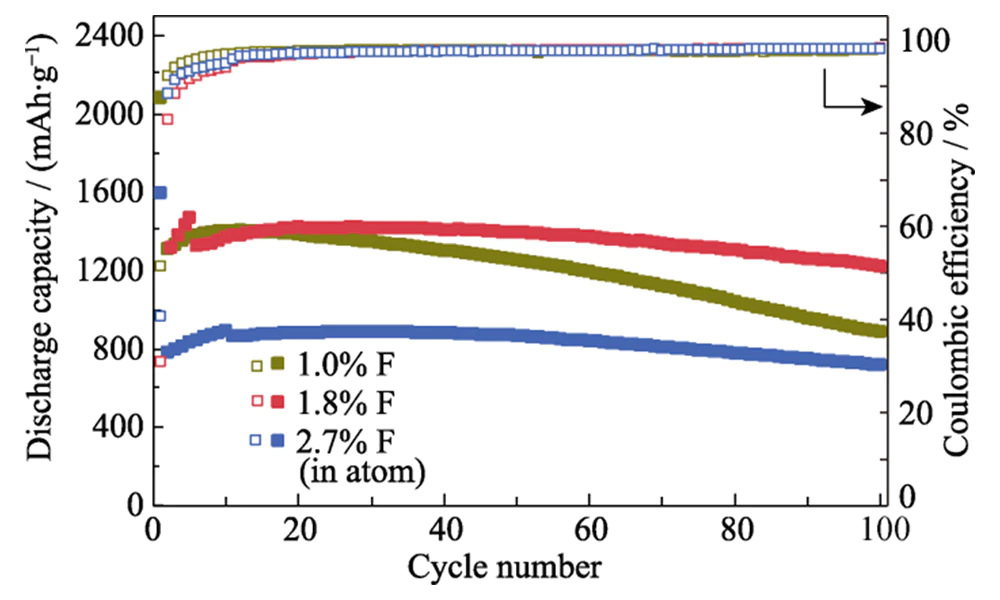
Afb. 6 Fietsstabiliteit van Si@C-F-anodes met verschillende F-verhoudingen bij een stroomdichtheid van 0,4 A·g-1 met anodes geactiveerd door 4-10 cycli bij 0,2 A·g-1 vóór de cyclus
De EIS-spectra van Si@C en Si@C-F anodes bestaan uit semi-boogcurven in het midden- tot hoogfrequente gebied hellende rechte lijnen in het laagfrequente gebied (Figuur 7 (a)). De halve boog curve in het midden- tot hoogfrequente bereik houdt verband met de ladingsoverdracht weerstand (Rct) en de hellende rechte lijn in het lage frequentiebereik weerspiegelt voornamelijk de Warburg-impedantie (ZW) van lithiumiondiffusie [26]. Vóór het opladen en ontladen, de Rct van Si@C-F en Si@C negatieve elektroden zijn vergelijkbaar, maar de eerste heeft een lagere ZW vanwege de zeer defecte met fluor gedoteerde koolstoflaag die het oppervlak bedekt. Na opladen en ontladen cycli is de Rct (5,51 Ω) van de Si@C-F-anode aanzienlijk lager dan die van de Si@C-anode (21,97 Ω) (Figuur 7(b)), en de ZW is veel lager dan de laatstgenoemd. Dit toont aan dat de fluorrijke SEI-grensvlakfilm geïnduceerd door de Met fluor gedoteerde koolstoflaag kan de grensvlaklading effectief verbeteren en transportmogelijkheden van lithiumionen.
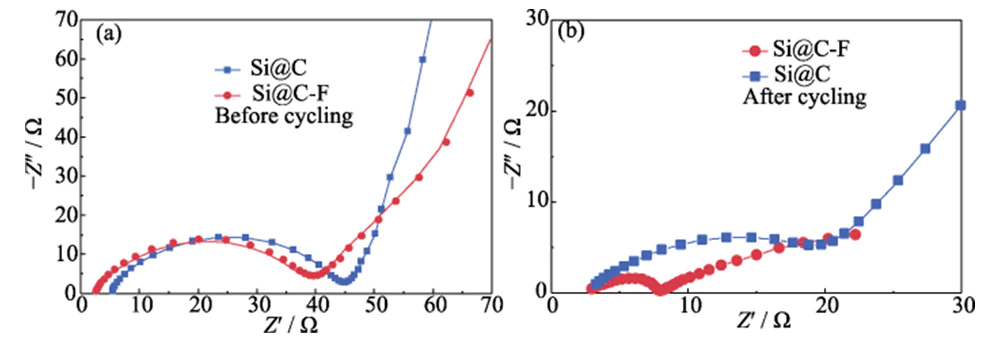
Afb. 7 Nyquist-grafieken van de Si@C- en Si@C-F-anodes (a) voor en (b) na het fietsen bij een stroomdichtheid van 0,4 A·g-1
2.3 Karakterisering van de elektrodestructuur na laden en ontladen
SEM-karakterisering na laden en ontladen cycli (Figuur 8(a~c)) laat zien dat dit te wijten is aan de aanzienlijke volume-expansie effect van silicium tijdens het lithiuminbrengproces, de dikte van de De Si@C-elektrode nam toe met 132,3%. Dit belemmert niet alleen de overdracht van ionen en elektronen, verhoogt de interne weerstand en polarisatie van de elektrode, maar veroorzaakt ook enorme mechanische spanningen, waardoor de elektrode breuk en gescheiden van de huidige collector, waardoor de prestaties van de Si@C-anode vervalt snel (Figuur 5 (c)). Ter vergelijking: de elektrode de dikte van de Si@C-F-anode nam na het opladen met slechts 26,6% toe ontladingscycli, en handhaafde een goede structurele stabiliteit van de elektrode (Figuur 8(d~f)). Hieruit blijkt dat de geïntroduceerde met fluor gedoteerde koolstoflaag dat wel kan effectief bufferen van het volume-expansie-effect van lithium-insertie in silicium materialen op microschaal, waardoor de structurele stabiliteit van de elektrode op de macroschaal van onder naar boven.
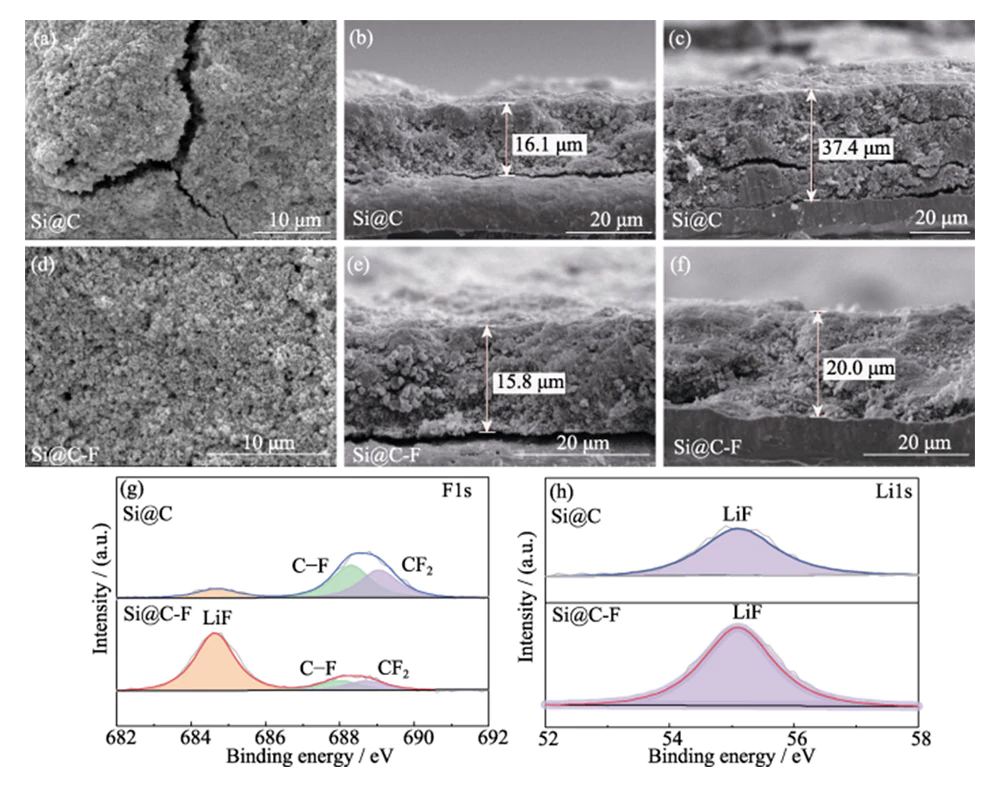
Afb. 8 Bovenste SEM-afbeeldingen van (a) Si@C en (d) Si@C-F anodes na het fietsen; SEM-afbeeldingen in dwarsdoorsnede van (b, c) Si@C en (e, f) Si@C-F anodes (b, e) voor en (c, f) na het fietsen; Hoge resolutie (g) F1s en (h) Li1s XPS-spectra van SEI op Si@C- en Si@C-F-anodes na fietsen
De samenstelling van de SEI-film op het oppervlak van Si@C en Si@C-F negatieve elektroden na laad- en ontlaadcycli werden geanalyseerd door XPS (Figuur 8(g~h)). In het F1s XPS-spectrum met hoge resolutie is de binding energiepieken bij de bindingsenergieën van 684,8, 688,3 en 689,1 eV komen overeen op respectievelijk LiF, C-F-obligaties en CF2. Dienovereenkomstig zijn er ook karakteristieke pieken die overeenkomen met LiF-soorten in de Li1s met hoge resolutie XPS-spectrum, wat aangeeft dat er een SEI-film met LiF-soorten wordt gevormd het oppervlak van de siliciumanode. Vergeleken met de Si@C-anode is het LiF-gehalte op het oppervlak van de Si@C-F-anode is hoger, wat aangeeft dat de LiF in de SEI-film ontstaat niet alleen door de ontleding van lithiumzouten in de elektrolyt, maar ook uit de F in de met fluor gedoteerde koolstoflaag. De vorming van LiF met hoge modulus kan de structurele sterkte effectief vergroten van de SEI-film en remmen de volumeverandering van lithiuminsertie in silicium materialen. Tegelijkertijd worden de brede bandafstand en isolerende eigenschappen van LiF gewaarborgd kan de SEI-dikte verminderen en het initiële onomkeerbare lithiumverlies verminderen. LixSi-legering, het lithieringsproduct van LiF en Si, heeft een hoog grensvlak energie en kan zich beter aanpassen aan de plastische vervorming van het gelithieerde silicium anode tijdens het fietsen, waardoor de fietsstabiliteit van de fiets verder wordt verbeterd elektrode [19].
3 Conclusie
In dit onderzoek met fluor gedoteerd Met koolstof beklede nano-siliciummaterialen werden bereid via een eenvoudige en laag-toxische gasfasefluoreringsmethode. Uit onderzoek blijkt dat fluordoping (1,8% F) vergroot enerzijds de defecten van de koolstofcoatinglaag het siliciumoppervlak en biedt daarbij overvloedige lithiumionentransportkanalen Nano-silicium is strak gecoat om de volume-expansie ervan te onderdrukken. Aan de andere kant Aan de andere kant wordt een zeer stabiele SEI-film, rijk aan LiF, op het oppervlak van het oppervlak geïnduceerd nano-siliciummateriaal, waardoor de stabiliteit en Coulomb-efficiëntie verder worden verbeterd van de siliciumanode. Dankzij dit is de eerste Coulombische efficiëntie van de Met fluor gedoteerde, met koolstof gecoate nano-siliciumanode verbeterd tot 65,9%. Bij een stroom dichtheid van 0,2 ~ 5,0 A · g-1, het vertoont een hoge specifieke capaciteit van 1540 ~ 580 mAh·g-1, en kan na 200 cycli 75% van de initiële capaciteit behouden. Dit werk levert nieuwe ideeën op voor het ontwerp en de constructie van siliciumanode materialen met hoge capaciteit en hoge stabiliteit.
Referentie
[1] NIU S S, WANG Z Y, YU M L, et al. MXene-gebaseerd elektrode met verbeterde pseudocapaciteit en volumetrische capaciteit voor type en lithiumopslag met ultralange levensduur.ACS Nano, 2018, 12(4): 3928.
[2] SU X, WU Q L, LI J C, et al. Op silicium gebaseerde nanomaterialen voor lithium-ionbatterijen: een recensie.Advanced Energy Materials, 2014, 4(1): 1300882.
[3] GE M Z, CAO C Y, GILL M B, et al. Recente ontwikkelingen in op silicium gebaseerde elektroden: van fundamenteel onderzoek naar praktijk toepassingen.Advanced Materials, 2021, 33(16): 2004577.
[4] LI P, ZHAO G Q, ZHENG X B, et al. Recente vooruitgang op het gebied van silicium anodematerialen voor praktische lithium-ionbatterijtoepassingen.Energie Opslagmaterialen, 2018, 15: 422.
[5] LIU X H, ZHONG L, HUANG S, et al. Grootte-afhankelijk breuk van siliciumnanodeeltjes tijdens lithiatie.ACS Nano, 2012, 6(2): 1522.
[6] LUO W, WANG Y X, CHOU S L, et al. Kritische dikte van fenol op hars gebaseerde koolstofgrenslaag voor het verbeteren van de stabiliteit bij lange cycli anodes van siliciumnanodeeltjes.Nano Energy, 2016, 27: 255.
[7] DOU F, SHI L Y, CHEN GR, Silicium/koolstof composiet anodematerialen voor lithium-ionbatterijen.Elektrochemische energiebeoordelingen, 2019, 2(1): 149.
[8] JIA H P, ZOU L F, GAO P Y, et al. Hoge prestaties siliciumanodes mogelijk gemaakt door onbrandbare gelokaliseerde hoge concentratie elektrolyten.Advanced Energy Materials, 2019, 9(31): 1900784.
[9] CHOI S H, KWON T W, COSKUN A, et al. Zeer elastisch bindmiddelen waarin polyrotaxanen zijn geïntegreerd voor anodes van siliciummicrodeeltjes in lithium ionenbatterijen.Wetenschap, 2017, 357: 279.
[10] LIZ H, ZHANG Y P, LIU TF F, et al. Siliciumanode met hoge initiële Coulomb-efficiëntie door gemoduleerd trifunctioneel bindmiddel voor lithium-ionbatterijen met hoge capaciteit. Geavanceerde energie Materialen, 2020, 10(20): 1903110.
[11] XU Z L, CAO K, ABOUALI S, et al.Studie van lithieringsmechanismen van hoogwaardig koolstofgecoat Si anodes door in-situ microscopie.Energy Storage Materials, 2016, 3: 45.
[12] TEKI R, MONI K D, RAHUL K, et al. Nanogestructureerde siliciumanodes voor oplaadbare lithium-ionbatterijen.Klein, 2009, 5(20): 2236.
[13] XIA S X, ZHANG X, LUO L L, et al. Zeer stabiel en ultrahoge Li-metaalanode mogelijk gemaakt door gefluoreerde koolstofvezels.Small, 2021, 17: 2006002.
[14] ZHANG S L, WANG X, HO K S, et al. Raman-spectra in a breed frequentiegebied van p-type poreus silicium.Journal of Applied Natuurkunde, 1994, 76(5): 3016.
[15] HUANG W, WANG Y, LUO G H, et al. 99,9% zuiverheid van meerwandige koolstofnanobuisjes door vacuüm gloeien bij hoge temperatuur. Carbon, 2003, 41(13): 2585.
[16] MCDOWELLM T, LEE S W, NIX W D, et al. 25e verjaardag artikel: inzicht in de lithiatie van silicium en andere legeringsanodes voor lithium-ionbatterijen.Advanced Materials, 2013, 25(36): 4966.
[17] SLEUTEL B, MORCRETTE M, TARASCON J M.Pair-distributiefunctieanalyse en solid-state NMR-studies van silicium elektroden voor lithium-ionbatterijen: inzicht in de (de)lithiatie mechanismen. Journal of American Chemical Society, 2011, 133(3): 503.
[18] GAO H, XIAO L S, PLUMEL I, et al. Parasitaire reacties op nanoschaal siliciumanodes voor lithium-ionbatterijen.Nano Letters, 2017, 17(3): 1512.
[19] CHEN J, FAN X L, LI Q, et al. Elektrolytontwerp voor LiF-rijk vaste-elektrolyt-interfaces om hoogwaardige anoden van micro-legeringen mogelijk te maken voor batterijen.Nature Energy, 2020, 5(5): 386.
[20] ZHANG P, GAO Y Q, RU Q, et al. Schaalbare bereiding van poreus nano-silicium/TiN@carbon-anode voor lithiumionbatterijen.Toegepast oppervlak Wetenschap, 2019, 498: 143829.
[21] SU M R, WAN H F, LIU Y J, et al. Meerlaags koolstofgecoat Si-gebaseerd composiet als anode voor lithium-ionbatterijen. Poeder Technologie, 2018, 323: 294.
[22] PU JB, QIN J, WANG Y Z, et al. Synthese van de micro-nanobolstructuur silicium-koolstofcomposiet als anodemateriaal voor lithium-ionbatterijen. Chemisch Physics Letters, 2022, 806: 140006.
[23] GAO R S, TANG J, YU XL, et al. Een sandwichachtige silicium-koolstof composiet bereid door oppervlaktepolymerisatie voor snelle opslag van lithiumionen.
Nano-energie, 2020, 70: 104444.
[24] GONG X H, ZHENG Y B, ZHENG J, et al.Yolk-shell silicium/koolstofcomposieten vervaardigd uit een aluminium-siliciumlegering als anode materialen voor lithium-ionbatterijen.Ionics, 2021, 27: 1939.
[25] LIA Y R, WANG R Y, ZHANG J W, et al.Sandwich structuur van met koolstof beklede silicium/koolstof nanovezelanodes voor lithium-ion batterijen.Ceramics International, 2019, 45: 16195.
[26] YANG X M EN ROGACH A L.Elektrochemische technieken in batterijonderzoek: een tutorial voor niet-elektrochemici.Advanced Energy Materials, 2019, 9(25): 1900747.



