Categorieën
nieuwe blog
- Handleiding voor de selectie van batterij-elektrolyten: wat inkoopmanagers moeten weten
- Apparatuur voor knoopcelbatterijlaboratoria: de complete checklist voor R&D-laboratoria voor batterijen
- Vergelijking van kathodematerialen voor batterijen: NMC, LFP en NCA
- Trends in de productie van lithium-ionbatterijen tot 2026: een B2B-kopersgids
- Stapsgewijze handleiding voor het productieproces van lithium-ionbatterijen
Tags
Mechanismen voor capaciteitsafname van lithium-ionbatterijen
Capaciteitsverlies in lithium-ionbatterijen wordt gecategoriseerd in omkeerbaar capaciteitsverlies en onomkeerbaar capaciteitsverlies. Omkeerbaar capaciteitsverlies is relatief "mild" en kan gedeeltelijk worden hersteld door het aanpassen van laad-ontlaadprotocollen (bijv. het optimaliseren van de laadstroom en spanningslimieten) en het verbeteren van de gebruiksomstandigheden (bijv. temperatuur-/vochtigheidsregeling). Onomkeerbaar capaciteitsverlies daarentegen ontstaat door onomkeerbare veranderingen in de batterij, wat leidt tot permanente capaciteitsvermindering. Volgens de GB/T 31484-2015-normen voor levensduurtests: "Tijdens standaard levensduurtests mag de ontlaadcapaciteit niet lager zijn dan 90% van de initiële capaciteit na 500 cycli, of 80% na 1000 cycli." Als de batterij binnen deze standaardcyclusbereiken een snelle capaciteitsafname vertoont, wordt dit geclassificeerd als capaciteitsvermindering, waarbij doorgaans sprake is van onomkeerbare degradatiemechanismen.
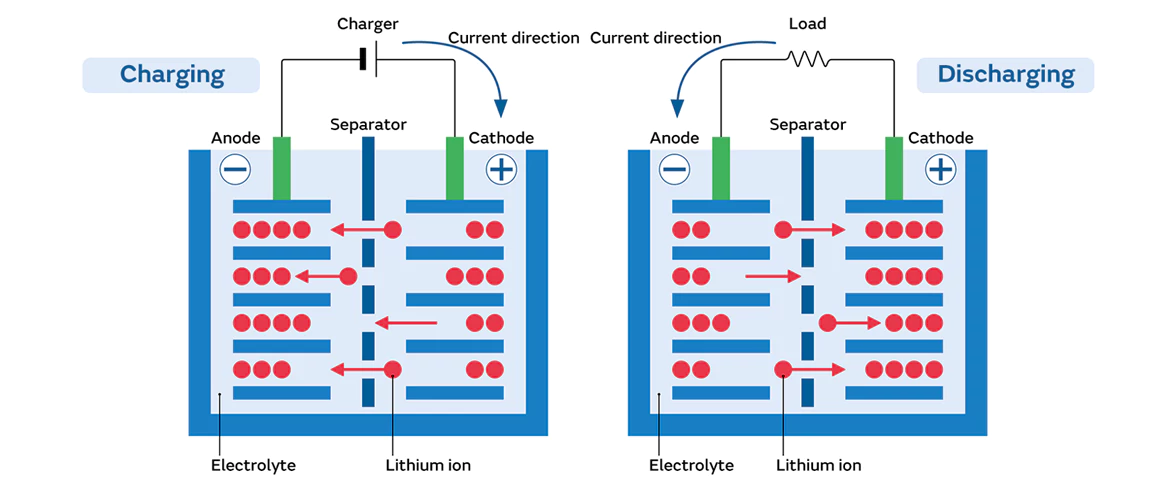
I. Materiaalgerelateerde factoren
1. Structurele degradatie van kathodemateriaal
Kathodematerialen ondergaan complexe fysische en chemische veranderingen tijdens laad-ontlaadcycli. Neem bijvoorbeeld spinelgestructureerd LiMn₂O₄: de structuur vervormt door het Jahn-Teller-effect tijdens de cycli. Deze vervorming neemt toe bij herhaalde cycli en kan uiteindelijk leiden tot breuk van kathodedeeltjes. Gebroken deeltjes verslechteren het elektrische contact tussen de deeltjes, waardoor het elektronentransport wordt belemmerd en de capaciteit afneemt. Bovendien treden in sommige kathodematerialen onomkeerbare faseovergangen en structurele verstoringen op. Zo gaan bepaalde kathodematerialen onder hoge spanning over van stabiele kristalstructuren naar fasen die ongunstig zijn voor de intercalatie/de-intercalatie van lithiumionen, waardoor de mobiliteit van lithiumionen wordt belemmerd en het capaciteitsverlies toeneemt.
2. Overmatige SEI-groei op anodeoppervlakken
Voor grafietanodes zijn de interacties tussen het oppervlak en de elektrolyt cruciaal. Tijdens het initiële laadproces ondergaan componenten in de elektrolyt reductiereacties op het grafietoppervlak, waardoor een vaste elektrolyt-interfaselaag (SEI) ontstaat. Normaal gesproken is de SEI-laag ionisch geleidend maar elektronisch isolerend, waardoor de anode wordt beschermd tegen continue elektrolytcorrosie. Overmatige SEI-groei brengt echter aanzienlijke problemen met zich mee. Ten eerste verbruikt SEI-vorming lithiumionen, waardoor de beschikbare Li⁺ voor normale laad- en ontlaadprocessen afneemt en capaciteitsverlies optreedt. Ten tweede kunnen overgangsmetaalverontreinigingen (bijvoorbeeld afkomstig van kathode-oplossing) die zich op het anodeoppervlak afzetten, verdere SEI-groei katalyseren, waardoor lithiumuitputting wordt versneld.Anodes op basis van silicium worden, ondanks hun hoge theoretische capaciteit, geconfronteerd met een sterke volume-expansie (>300%) tijdens de lithiëring/delithiëring. Herhaalde expansie/contractie veroorzaakt structurele schade, elektrodeverpulvering en verlies van elektrisch contact, wat leidt tot onomkeerbaar capaciteitsverlies. Hoewel technologieën zoals nanogestructureerde siliciumanodes en silicium-koolstofcomposieten volume-effecten beperken, blijft dit een cruciale uitdaging voor de commercialisering van siliciumanoden.
3. Ontleding en afbraak van elektrolyten
De elektrolyt speelt een cruciale rol in ionentransport. Veelvoorkomende lithiumzouten zoals LiPF₆ vertonen een slechte chemische stabiliteit en ontbinden bij hoge temperaturen of spanningen, waardoor de beschikbare hoeveelheid Li⁺ afneemt en schadelijke bijproducten ontstaan (bijv. PF₅, dat reageert met oplosmiddelen). Sporenvocht in de elektrolyt reageert met LiPF₆ en produceert waterstoffluoride (HF), een corrosief middel dat kathode-/anodematerialen en stroomcollectoren aantast. Slechte afdichting van de batterij maakt het binnendringen van vocht/zuurstof van buitenaf mogelijk, wat de oxidatie van de elektrolyt versnelt. Gedegradeerde elektrolyten vertonen een verhoogde viscositeit, verkleuring en een drastisch verminderde ionengeleiding, wat de batterijprestaties ernstig verslechtert.
4. Corrosie van de stroomcollector
Stroomcollectoren (bijvoorbeeld aluminiumfolie voor kathodes, koperfolie voor anodes) verzamelen en geleiden stroom. Storingen kunnen onder meer corrosie en verminderde hechting veroorzaken. Corrosiemechanismen omvatten:• Chemische corrosie: HF uit elektrolytnevenreacties reageert met collectoren, waardoor slecht geleidende verbindingen worden gevormd die de grensvlakweerstand verhogen.
• Elektrochemische corrosie: Bij koperfolie-anoden vindt oplossing plaats bij lage potentialen. Opgeloste koperionen migreren en slaan neer op kathodes ("koperplating"), waardoor de collectordoorsnede kleiner wordt en nevenreacties ontstaan.
• Adhesiefalen: volumeveranderingen tijdens de cyclus kunnen ervoor zorgen dat actieve materialen loskomen van de collectoren als de adhesie onvoldoende is, waardoor ze elektrochemisch inactief worden.
5. Sporen van onzuiverheden in het batterijsysteem
Onzuiverheden in overgangsmetalen (Fe, Ni, Co) die via grondstoffen worden geïntroduceerd, kunnen deelnemen aan redoxreacties, de afbraak van elektrolyten katalyseren of concurreren met Li⁺-intercalatie. Deze onzuiverheden destabiliseren ook SEI-lagen, waardoor anodereacties verergeren.
II. Operationele omgevingsfactoren
1. Temperatuureffecten
• Hoge temperaturen versnellen de afbraak van elektrolyten en de herstructurering van SEI. De afbraak van LiPF₆ genereert PF₅, dat reageert met oplosmiddelen, terwijl SEI-lagen dikker worden tot anorganisch gedomineerde films met een hogere ionenweerstand. Elektrische voertuigen die in warme klimaten rijden, vertonen bijvoorbeeld een versnelde capaciteitsvermindering.• Lage temperaturen verhogen de viscositeit en polarisatie van de elektrolyt, wat de vorming van lithium op anodes bevordert. Lithiumdendrieten kunnen separatoren doorboren en interne kortsluiting veroorzaken.
2. Laad-ontlaadsnelheden (C-snelheden)
Hoge C-waarden tijdens het opladen veroorzaken een ongelijkmatige lithiumafzetting, waardoor dendrieten ontstaan die Li⁺ verbruiken en interne kortsluiting veroorzaken. Ontladen met hoge snelheid verergert de polarisatie, waardoor de bruikbare energie afneemt en het capaciteitsverlies toeneemt. Elektrisch gereedschap dat frequent met hoge stroom ontlaadt, heeft een kortere levensduur.
3. Overladen/Te veel ontladen
• Overbelasting zorgt voor overmatige delithiatie van kathodes, wat leidt tot een structurele ineenstorting en heftige oxidatie van de elektrolyt (gasontwikkeling, zwelling of thermische runaway).• Overontlading zorgt voor overmatige lithiëring van anodes, waardoor hun structuur destabiliseert en elektrolytreductie optreedt. Vroege smartphones zonder beveiligingscircuits vertoonden een snel capaciteitsverlies bij dergelijk misbruik.
Gevolgen van batterijstoring
Ernstige capaciteitsvermindering manifesteert zich als onvoldoende looptijd (bijv. kortstondig gebruik van het apparaat na het opladen) of abnormaal laadgedrag (bijv. langzaam opladen). In kritische toepassingen:
• Elektrische voertuigen: een defecte accu vermindert de actieradius en kan leiden tot gestrande voertuigen.• Energieopslag op netniveau: defecte batterijen verstoren de betrouwbaarheid van de stroomvoorziening en vormen een bedreiging voor de veiligheid van het net.



